
Abstrak
Amonia disintesis secara industri melalui katalis berbasis Fe yang dipromosikan secara ganda selama lebih dari satu abad. Meskipun sintesis amonia mencerminkan reaksi katalitik prototipikal, desain katalis rasional masih mustahil karena kompleksitas struktural penuh dari sistem katalis ini yang sering disebut sebagai besi amonia dan keterikatan strukturalnya hampir tidak dipahami. Di sini, struktur mesoskopik dari katalis sintesis amonia yang dipromosikan secara ganda secara teknis diungkap menggunakan pendekatan mikroskopi elektron penjembatan skala yang dilengkapi dengan difraksi sinar-X dan spektroskopi untuk mengeksplorasi integritas struktural besi amonia. Kontribusi dan struktur amorf dari jenis melilit dan trikalsium aluminat sebagai fase tambahan diidentifikasi. Lebih jauh, pemahaman tentang keluarga besi amonia dengan mengungkap peran perimeter Fe-platelet, kerangka Fe, lapisan tipis Fe, dan Fe refraktori diperluas. Keterkaitan mereka disorot, yang menunjukkan bahwa setiap komponen harus ada untuk memenuhi tugas tertentu. Studi ini menunjukkan bahwa ilmu katalisis hanya dapat berlanjut jika secara terbuka mengeksplorasi kompleksitas penuh sistem katalitik.
1 Pendahuluan
Dengan produksi tahunan >182 juta metrik ton, [ 1 , 2 ] amonia (NH 3 ) menyuburkan dunia karena membentuk dasar pupuk berbasis nitrogen. Lebih jauh lagi, amonia juga dianggap sebagai salah satu molekul yang paling menjanjikan untuk penyimpanan dan pengangkutan hidrogen sebagai bagian dari lanskap energi berkelanjutan. [ 3 – 5 ] Selama lebih dari satu abad, NH 3 diproduksi secara industri melalui proses Haber Bosch di atas katalis berbasis besi (Fe), masih mengikuti resep yang didasarkan pada sintesis lelehan dengan adanya beberapa oksida promotor, termasuk kalium (K), aluminium (Al), kalsium (Ca), dan silikon (Si) [ 6 – 8 ] dengan pengecualian bahwa dalam formulasi modern, prekursor magnetit telah digantikan sebagian oleh wüstite. [ 9 ]
Formulasi kompleks katalis tersebut ditemukan secara empiris oleh Alwin Mittasch yang menambahkan bijih magnetit beku dari Gällivare – sebuah wilayah di Swedia yang memiliki bijih besi dengan kandungan K hingga 3 wt.-% – ke dalam salah satu reaktor uji di BASF. [ 10 , 11 ] Struktur khusus bijih tersebut segera dikenali dan material tersebut ditemukan berbutir dan rapuh, nonmagnetik, dan membentuk spons logam berpori setelah aktivasi. Faktanya, sifat-sifat ini tidak biasa untuk sampel magnetit dan dapat menjelaskan mengapa ≈4.000 upaya sintesis dan >10.000 uji katalitik diperlukan untuk mereproduksi mineral ini. [ 11 ]
Penasaran dengan temuan tersebut, Fritz Haber menulis kepada dewan direksi di BASF: “[…] Sungguh luar biasa bagaimana keanehan baru selalu muncul dalam berbagai hal. Besi yang awalnya digunakan Ostwald, dan yang kemudian kami coba ratusan kali dalam keadaan bersih, kini bekerja dalam keadaan tidak bersih. Saya menyadari lagi bagaimana seseorang harus mengikuti setiap petunjuk sampai akhir. Percobaan dengan mangan, yang saya gambarkan dengan Le Rossignol dalam naskah yang Anda bagikan, dan di mana mangan bekerja dengan sangat cemerlang tanpa pernah berhasil mereproduksi aktivitas ini, kini terbukti dengan sendirinya.” [ 11 ]
Dalam literatur terkini, besi yang tidak bersih ini disebut sebagai besi amonia. Meskipun besi amonia dianggap sebagai kunci produksi industri NH3 yang efisien , ia masih merupakan salah satu senyawa yang paling kontroversial yang dibahas dalam ruang fasa besi. Surat Fritz Haber yang dirumuskan pada tahun 1910 telah menyatakan bahwa sistem model kristal tunggal tidak cocok untuk menggambarkan secara komprehensif struktur katalis sintesis amonia teknologi. Akan tetapi, pemanfaatannya mungkin dapat dibenarkan karena mereka membantu memperoleh beberapa pemahaman mendasar tentang reaksi ini, yang masih berlaku. Dari penelitian tersebut, disimpulkan bahwa permukaan Fe(111) dapat mengaktifkan N2 paling cepat, sementara permukaan Fe(110) memiliki aktivitas paling sedikit dan bahwa langkah penentu laju adalah disosiasi N2 . [ 12-19 ] Lebih jauh , situs C7, tempat atom Fe yang menyerap dikelilingi oleh tujuh tetangga terdekat, ditemukan sebagai yang paling penting. [ 20-22 ] Selain itu , telah ditunjukkan bahwa spesies N yang berbeda hadir di permukaan selama reaksi . [ 23 ] Perlu diketahui bahwa keunikan mekanisme reaksi ini belum terbukti secara eksperimental dan mungkin saja model kinetik juga berlaku untuk mekanisme reaksi berbeda yang mungkin terjadi secara bersamaan dalam formulasi teknis yang kompleks.
Pentingnya menganalisis kompleksitas kimia dalam katalis sintesis amonia teknis telah dihidupkan kembali, [ 18 ] karena mungkin juga penting untuk sintesis elektrokatalitik amonia, [ 24 , 25 ] dan awalnya berpusat di sekitar diskusi tentang parakristalinitas anisotropik yang berfokus pada apakah hercynite molekuler (Fe 2 AlO 4 ) atau blok penyusun Al 2 O 3 yang menyebabkan besi tidak bersih. [ 26 – 29 ] Peningkatan alat analitis pada awal abad ke-21 telah menyebabkan kebangkitan dalam investigasi struktural reaksi katalitik prototipikal ini, termasuk pengamatan regangan dalam kisi Fe dengan difraksi sinar-X (XRD) dan difraksi neutron in situ. [ 7 , 30 , 31 ] Namun, gambaran komprehensif tentang struktur katalis sintesis amonia teknis masih hilang karena teknik-teknik ini integral dan bergantung pada hamburan yang koheren.
Terinspirasi oleh deskripsi bijih magnetit dari wilayah Gällivar yang diberikan oleh Alwin Mittasch, kami mengusulkan bahwa kompleksitas dalam sistem katalis ini merupakan sifat struktural intrinsik yang meluas ke berbagai skala panjang dan disesuaikan dengan pemilihan paket promotor yang memadai. Paket promotor ini multifungsi, menjadi penentu fungsi katalitik dan stabilitas jangka panjang, dan akhirnya bertanggung jawab untuk membangun dan menstabilkan struktur kerja. [ 18 , 28 , 32 , 33 ]
Di sini, kami menyediakan analisis struktur multi-moda, skala-bridging dari prekursor dan katalis sintesis amonia teknis berbasis wüstite multi-promoted yang diaktifkan dengan menggabungkan hasil dari XRD, mikroskopi elektron, serta spektroskopi elektron dan sinar-X. Seperti yang akan kami tunjukkan, katalis sintesis amonia teknis adalah mahakarya mesoteknologi. Dalam konteks ini, istilah “meso” tidak hanya merujuk pada skala panjang antara nano dan makro, tetapi juga mesokimia, yang mengarah pada bahan terstruktur hierarkis dengan sifat unik yang menarik paralel dengan enzim atau tulang. [ 34 ] Kami mengungkap integritas struktural besi amonia, yang akan diperluas oleh empat konstituen dependen skala panjang: perimeter platelet-Fe, kerangka Fe, lapisan tipis Fe, dan Fe refraktori. Satu fraksi amorf tambahan dan dua fase promotor kristal tambahan, trikalsium aluminat dan tipe struktur melilite, telah diidentifikasi yang tampaknya penting untuk kinerja dan stabilitas jangka panjang sistem ini. Struktur baru ini melengkapi pengetahuan yang ada tentang besi amonia. Struktur ini saling terkait erat dan bertanggung jawab atas kisah sukses katalis sintesis amonia berbasis Fe.
2 Hasil
2.1 Prekursor Berbasis Wüstite
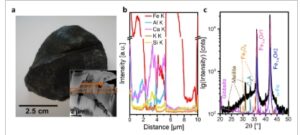
Prekursor katalis sintesis amonia berbasis wüstite yang dipromosikan secara multi-dibuat dengan sintesis lelehan, yang menghasilkan batuan padat dan tidak berpori, yang mana oksida besi merupakan komponen utamanya, setelah pendinginan hingga suhu kamar ( Gambar 1 a ). Analisis lebih lanjut dari mikrostruktur prekursor ini dengan mikroskop elektron transmisi pemindaian (STEM) menunjukkan distribusi yang tidak seragam dari unsur-unsur yang terlibat seperti yang ditunjukkan oleh pemisahan kontras gambar menjadi daerah yang lebih gelap dan lebih terang (Gambar 1a , sisipan). Pemindaian garis spektroskopi sinar-X dispersif energi (EDX) (Gambar 1b ) menunjukkan bahwa daerah yang lebih terang berhubungan dengan domain wüstite kaya-Fe, sedangkan daerah yang lebih gelap dicirikan oleh koeksistensi unsur-unsur promotor Al, Ca, K, dan Si disertai dengan oksigen. Konsentrasi promotor ini dapat bervariasi secara lokal dan promotor seperti urat ini mengikat butiran wüstite yang berbeda. Lebih jauh, Al, Ca, dan K juga dapat ditemukan di beberapa butiran wüstite. Analisis ini sudah menyiratkan bahwa prekursor untuk katalis sintesis amonia teknis bersifat heterogen dan kompleks dalam hal komposisi dan struktur.
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
Kompleksitas prekursor dalam katalis sintesis amonia teknis yang dipromosikan secara multipel: a) Gambar potongan “batu wüstite” yang dipadamkan setelah sintesis lelehan dan gambar STEM ikhtisar lamela tipis yang disiapkan oleh berkas ion terfokus (FIB) yang menunjukkan variasi kontras pada skala mikro (sisipan); b) Pemindaian garis EDX (kiri ke kanan) dari area oranye yang disorot dalam sisipan yang menampilkan kompleksitas komposisi lokal prekursor; c) Pola XRD dan kecocokan Rietveld dari prekursor berbasis wüstite menggunakan radiasi Cu Kα.
Untuk lebih mengeksplorasi keragaman struktur, pengukuran difraksi sinar-X (XRD) dilakukan. Pola XRD dari prekursor berbasis wüstite (Gambar 1c ; Gambar S1 , Informasi Pendukung) menguatkan kompleksitas yang ditemukan oleh analisis komposisi lokal (Gambar 1b ). Selain wüstite, sedikitnya tujuh fase berbeda telah diidentifikasi dalam formulasi teknis, termasuk halo amorf, magnetit (Fe3O4 ) , Fe metalik, fase tipe trikalsium aluminat (Ca3Al2O6 , C3A ) , tipe struktur melilite – larutan padat antara gehlenite kaya Al (Ca2Al [ AlSiO7 ] dan åkermanite kaya Mg (Ca2Mg [ Si2O7 ] ) – dan gibbsite (γ-Al(OH) 3 ) . Parameter kisi dan fraksi berat yang sesuai (relatif terhadap jumlah fase kristal) yang dihitung dari fraksi massa yang diperoleh dengan penyempurnaan Rietveld disajikan dalam Tabel 1. Meskipun berbagai fase berbeda telah diidentifikasi, fase dominan prekursor masih wüstite (Fe1 − xO , total 91,7 wt.%). refleksi wüstite menunjukkan profil puncak asimetris, dengan ekor yang menonjol pada sisi sudut yang lebih tinggi, sehingga menunjukkan distribusi yang luas dalam ukuran domain kristalit dan parameter kisi (Gambar S1 , Informasi Pendukung). Oleh karena itu, pola tersebut didekati dalam analisis Rietveld menggunakan dua fase tipe wüstite. Namun, pendekatan ini tidak dimaksudkan untuk menyiratkan keberadaan sebenarnya dari dua spesies wüstite diskrit, tetapi lebih digunakan sebagai solusi untuk menangani distribusi yang mungkin kontinu dalam kemungkinan terbatas dari metode Rietveld. Kami menafsirkannya sebagai gradien kontinu dalam stoikiometri Fe 1− x O yang muncul antara Fe 0,95 O dan Fe 0,93 O.
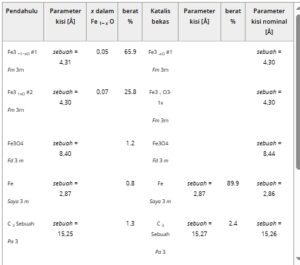
Tabel 1. Parameter kisi dan fraksi fase untuk prekursor sintesis amonia teknis dan katalis teraktivasi setelah operasi pada suhu 500 °C, 96 jam, 90 bar, N 2 : H 2 = 1:3 yang diperoleh dari pemurnian Rietveld dengan mengabaikan fase amorf.
2.2 Sifat Massal Katalis yang Diaktifkan
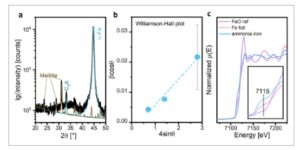
Integritas fase berubah sepenuhnya setelah memaparkan prekursor selama 96 jam pada kondisi sintesis amonia pada 90 bar. Rincian tambahan mengenai efek promotor dan pentingnya aktivasi katalis ini dalam kondisi sintesis amonia dapat ditemukan dalam laporan kami sebelumnya. [ 33 ] Kinerja katalitik yang sesuai selama sintesis amonia 96 jam diilustrasikan dalam Gambar S2 (Informasi Pendukung). Pola XRD yang sesuai ( Gambar 2 a ) menunjukkan kontribusi amorf, yang kontribusinya diredam dibandingkan dengan prekursor, dan tiga fase berbeda: α-Fe, C 3 A, dan melilite.
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
Analisis integral berbasis sinar-X dari katalis sintesis amonia teknis teraktivasi yang dipromosikan secara multipel setelah operasi pada suhu 500 °C, 96 jam, N 2 : H 2 = 1:3, 90 bar: a) Pola XRD dan kecocokan Rietveld dari katalis teraktivasi menggunakan radiasi Cu Kα; b) Plot Williamson-Hall menggunakan radiasi Mo Kα. Titik-titik padat mewakili hasil eksperimen. Garis putus-putus menunjukkan kecocokan linier. Batang galat dihitung dari kecocokan linieritas; c) Spektrum penyerapan sinar-X Fe K-edge yang dinormalkan di dekat struktur tepi (XANES) dari katalis teknis teraktivasi dan struktur pra-tepinya (sisipan) bersama dengan referensi foil Fe dan FeO.
Penggabungan heterocompound ke dalam α-Fe menginduksi regangan ke dalam kisi, yang dapat ditangkap oleh plot Williamson-Hall (WH). Plot WH dari keluarga refleksi hh 0 yang diperoleh menggunakan sumber sinar-X Mo ditunjukkan pada Gambar 2b dan pola XRD yang sesuai dianalisis dengan model regangan anisotropik disajikan pada Gambar S3 (Informasi Pendukung). Kemiringan pada Gambar 2b juga menunjukkan keberadaan regangan. [ 35 ] Ini membedakan besi amonia dari α-Fe murni. [ 31 ] Regangan anisotropik dalam senyawa bcc sulit untuk dirasionalisasi dan mungkin memiliki asal kimia yang berbeda, termasuk reduksi atau ekspansi yang lebih disukai dari orientasi tertentu yang disebabkan oleh keberadaan heteroelemen, kimia cacat yang berbeda, ukuran atau bentuk butiran, dan tekstur. [ 36 , 37 ] Pengukuran spektroskopi serapan sinar-X (XAS) dari tepi K Fe mengonfirmasi bahwa bcc metalik Fe adalah fase dominan dalam katalis yang diaktifkan (Gambar 2c ). Meskipun demikian, spektrum yang diperoleh berbeda secara nyata dari spektrum referensi foil Fe. Secara khusus, fitur pra-tepi pada 7115 eV (Gambar 2c , sisipan) lebih tinggi untuk katalis yang diaktifkan. Amplitudo osilasi pasca-tepi, pada gilirannya, ditekan, sementara frekuensinya cocok dengan referensi foil Fe. Distorsi spektrum yang diukur dalam transmisi tersebut umum terjadi pada sampel dengan ketebalan yang tidak homogen. Dengan demikian, kami mengaitkan perbedaan ini dengan variasi kerapatan sampel pada skala mikrometer, dan, dengan demikian, perbedaan tersebut dapat dikaitkan dengan ukuran butiran. Perbedaan tersebut selanjutnya menunjukkan bahwa istilah besi amonia mencakup skala panjang yang berbeda. Hal ini menggarisbawahi multidimensi Fe dalam formulasi teknis, yang ingin kami uraikan sebagai berikut.
2.3 Analisis Struktural Skala-Menjembatani
Kami pertama-tama menyelidiki asal-usul regangan anisotropik dalam mikrostruktur dengan menganalisis data dari mikroskop elektron pemindaian (SEM). Pada skala mikro, gambar SEM ( Gambar 3 ) menampilkan pluralisme morfologi di permukaan katalis ini. Mirip dengan laporan sebelumnya, butiran kaya-Fe yang sangat berpori (Gambar 3a , daerah yang lebih cerah) disatukan oleh fase promotor (daerah yang lebih gelap) yang berjalan melalui katalis yang diaktifkan dengan cara seperti urat. Selain itu, kerak menutupi sebagian permukaan butiran kaya-Fe yang berpori (Gambar 3b,c ; Gambar S4a,b , Informasi Pendukung). Pemetaan unsur (Gambar 3d ; Gambar S5 , Informasi Pendukung) menunjukkan bahwa kerak tersusun dari unsur-unsur promotor, yang menyiratkan bahwa perimeter besi promotor-amonia yang besar diproduksi. Seperti yang ditunjukkan pada Gambar 3c,d cakupan dapat dinyatakan oleh trombosit yang menutupi permukaan butiran Fe. Terakhir, Gambar 3e juga menunjukkan bahwa inklusi lokal dari fase tambahan kadang-kadang diamati pada permukaan butiran Fe yang berpori. Analisis SEM ini sudah menyoroti kompleksitas dan heterogenitas yang ada pada permukaan sistem katalis ini. Akibatnya, interaksi struktural yang penting antara fase promotor dan butiran yang kaya Fe akan terlewatkan oleh eksperimen perataan struktural. Pada skala mikro, besi amonia dicirikan oleh entitas berpori yang merupakan komposit dari platelet permukaan yang menutupi domain Fe sehingga menimbulkan perimeter platelet-besi yang meningkat.

Gambar 3
Buka di penampil gambar
Kekuatan Gambar
Karakteristik skala mikro besi amonia: Analisis SEM dari struktur mikro permukaan katalis sintesis amonia multi-promosi teknis: a) Vena promotor yang mengikat butiran kaya Fe bersama-sama; b,c) Platelet seperti kerak terbentuk di permukaan katalis ini selama sintesis amonia. Garis putus-putus pada (b) mewakili perimeter platelet (kerak)-besi. d) Spektroskopi sinar-X dispersif energi (EDX) yang menunjukkan bahwa kerak tersusun dari unsur-unsur promotor; “SE” mewakili gambar SEM. e) Inklusi lokal dari fase tambahan dalam matriks Fe berpori.
Uraian di atas difokuskan pada fitur permukaan, tetapi detail struktural penting yang berkontribusi pada besi amonia dalam bagian berpori dari katalis ini masih tersembunyi. Gambar SEM menyoroti porositas tinggi dan menunjukkan keberadaan lembaran Fe berlapis dalam bagian tersebut (Gambar 3e ; Gambar 4 a ; Gambar S4 , Informasi Pendukung). Struktur berpori tersebut diperkuat oleh pencitraan annular dark-field STEM (ADF-STEM) dari lamela yang disiapkan oleh berkas ion terfokus (FIB) dari katalis yang diaktifkan, yang menonjolkan bahwa bagian berpori dari katalis yang diaktifkan tersusun dari kerangka yang saling terjalin (Gambar 4b ). Sifat berpori dari bagian katalis juga konsisten dengan gambar TEM bright-field (BF) yang menunjukkan bahwa kerangka yang saling terjalin membentuk fondasi yang mendukung seluruh struktur katalis (Gambar 4c,d ; Gambar S6 , Informasi Pendukung). Selain itu, perubahan kontras lokal menunjukkan variasi skala nano yang parah dalam kondisi difraksi katalis yang diaktifkan, yang mencerminkan sifat material ini yang sangat rusak. Pengindeksan transformasi Fourier Cepat (FFT, Gambar 4e , sisipan) yang direkam dari gambar HR-TEM yang disajikan pada Gambar 4d menunjukkan bahwa rangka tersebut tersusun dari Fe metalik, yang didominasi oleh bidang kisi (110). Untuk memperoleh wawasan tentang kristalinitas bidang kisi ini, FFT terbalik (iFFT) telah dihitung untuk keluarga refleksi (110), yang disajikan pada Gambar 4f , yang menunjukkan distribusi spasialnya. Seperti yang ditunjukkan pada Gambar 4f , bidang kisi (110) tidak berkesinambungan dan sangat terputus-putus. Kami menginterpretasikan gambar ini sebagai visualisasi parakristalinitas dalam α-Fe. [ 26 ] Dalam struktur parakristalin seperti itu, atom-atom tersusun dalam pola teratur pada jarak pendek, tetapi tatanan ini tidak meluas pada jarak jauh. [ 38 ] Hal ini kontras dengan munculnya bidang kisi yang diharapkan dari model kristal tunggal, yang berkesinambungan, yang menunjukkan sifat material yang cacat dan keberadaan antarmuka padat-padat pada skala atom. Antarmuka ini dapat memodulasi pasokan heteroelemen melalui Fe melalui difusi. [ 39 – 41 ] Hal ini dapat menjadi penting karena dapat meregenerasi daerah aktif dan berkontribusi pada umur panjang sistem katalis ini dalam kondisi reaksi industri yang keras. Lebih jauh, area yang diperbesar diambil dari daerah yang diinginkan pada Gambar 4fmenunjukkan penampakan lokal bidang-bidang di antara 110 bidang kisi, yang menyiratkan bahwa bidang-bidang kisi digeser setengah sel satuan (Gambar 4g ). Harap perhatikan bahwa gambar TEM memberikan representasi 2D dari objek 3D. Dengan demikian, gambar ini juga dapat diinterpretasikan sebagai tumpukan 3D lapisan Fe. Karakter lapisan Fe selanjutnya diperkuat oleh temuan pinggiran Moire dalam mikrograf TEM (Gambar 4g ). Pola moire akan terbentuk jika bidang kisi yang berbeda atau bidang kisi yang sama, tetapi diputar, saling tumpang tindih. [ 33 , 42 , 43 ] FFT dan iFFT dari daerah yang sama menunjukkan bahwa 110 bidang kisi dan 200 bidang kisi hidup berdampingan (Gambar 4h,i ). Selain itu, beberapa refleksi 110 dan 200 ditemukan dalam FFT yang diputar sebesar ≈10°, yang mendukung karakter berlapis dari besi amonia (Gambar S7 , Informasi Pendukung). Pada skala nano, besi amonia didominasi oleh besi rangka yang tidak hanya membentuk tulang punggung sistem katalis, tetapi juga dicirikan oleh kompleksitas dan cacat ekstrem yang tampaknya diperlukan untuk menstabilkan fase berpori aktif.

Gambar 4
Buka di penampil gambar
Kekuatan Gambar
Karakterisasi rangka Fe: Fe berlapis dalam katalis sintesis amonia multi-promosi teknis yang diaktifkan pada skala panjang yang berbeda setelah operasi pada 500 °C, 96 jam, N 2 : H 2 = 1:3, 90 bar: a) Gambar SEM dari penampang yang memungkinkan pemeriksaan fase anisotropik yang terekspos; b) Gambar ADF-STEM dari lamela yang disiapkan FIB dari katalis yang diaktifkan yang menunjukkan bahwa bagian berpori dibentuk oleh jaringan Fe anisotropik yang terjalin; c) Gambar ikhtisar TEM dari katalis yang diaktifkan dengan kontras difraksi; d) Gambar HR-TEM dari rangka Fe di sekitar pori-pori; e) Gambar iFFT dari keluarga refleksi 110 yang menyoroti karakter parakristalin dari Fe berlapis. Sisipan menampilkan FFT dari gambar HR-TEM yang disajikan dalam (d); f) daerah yang diperbesar dari iFFT yang disajikan dalam (e); g) Gambar HR-TEM dari rangka Fe yang menampilkan pola Moire; Sisipan yang menunjukkan FFT dari (g) dengan penugasan FFT yang disajikan pada Gambar S7 (Informasi Pendukung); h) Gambar iFFT RGB dari pantulan yang sesuai dengan bidang yang berbeda dalam keluarga pantulan (110); i ) Gambar iFFT RGB dari pantulan yang sesuai dengan bidang yang berbeda dalam keluarga pantulan 200.
Pada skala atom, kami menemukan bahwa beberapa kerangka Fe dalam massa berpori ditutupi oleh lapisan tipis, tetapi padat dan sebagian amorf yang dapat terpapar pada fase gas ( Gambar 5 ; Gambar S6 , Informasi Pendukung). Gambar HR-TEM dikarakterisasi oleh material yang menunjukkan kontras yang lebih gelap dan lebih lemah. Ini mungkin berasal dari kontras massa-ketebalan, yang menyiratkan bahwa material dengan kontras yang lebih lemah, yang meluas ke dalam pori-pori, relatif tipis, sedangkan bagian yang lebih gelap sesuai dengan kerangka Fe. Pemeriksaan terperinci dari parameter kisi lokal yang diperoleh dari analisis FFT menunjukkan bahwa bidang kisi besi pada beberapa kesempatan sedikit diperbesar dibandingkan dengan nilai rata-rata yang diperoleh dari analisis XRD (Tabel 1 ; Gambar S8 , Informasi Pendukung). Misalnya, untuk bidang Fe(110) (d = 0,206 nm, nilai nominal 0,203 nm) dan (211) (d = 0,120 nm, nilai nominal 0,117 nm), deviasinya tidak signifikan dan berada dalam kesalahan pengukuran. Sebaliknya, untuk bidang kisi Fe (200) (d = 0,151 nm, nilai nominal 0,143 nm), peningkatan yang jelas diamati. Selain itu, lapisan tipis yang sangat cacat menutupi sebagian pori-pori dan melapisi dinding kerangka Fe. Kehadiran lapisan tipis di dalam pori-pori mungkin menunjukkan gangguan turbostratik lapisan Fe dalam kerangka Fe. Mereka dapat ditugaskan ke bidang kisi 200 yang sangat tegang dari α-Fe (Gambar 5a ) yang disebutkan sebelumnya, tipe struktur melilite (Gambar 5b ), serta koeksistensi fase amorf dengan C3A dan α-Fe (Gambar 5c ). Parameter kisi yang sedikit lebih besar dari bidang kisi (110) kerangka Fe dan bidang kisi (200) yang sangat terdistorsi yang diamati dalam besi film tipis menguatkan penggabungan anisotropik heteroelemen dari promotor ke dalam sebagian besar α-Fe yang menjadi ciri parakristal. Lebih jauh, distribusi unsur yang diperoleh dengan menggabungkan pencitraan STEM dengan spektroskopi kehilangan energi elektron (EELS, Gambar 5d–f ) menunjukkan bahwa Fe terletak di daerah luar dan dalam. Rasio intensitas garis putih L3-ke-L2 yang sesuai dari tepi Fe di area yang sama menunjukkan keadaan oksidasi Fe (Gambar S9 , Informasi Pendukung). Rasio yang rendah menyiratkan spesies Fe seperti logam yang ditemukan di bagian dalam sementara rasio yang tinggi seperti yang ditunjukkan di daerah luar mewakili spesies Fe teroksidasi. Bagian luar ini sebagian besar terdiri dari Ca, Fe teroksidasi, dan O yang menutupi inti logam Fe dengan kerak setebal ≈10 nm, menunjukkan terbentuknya struktur dari tipe melilite atau C 3Solusi yang solid. Pada skala atom, kontribusi tambahan dari besi amonia meluas ke Fe parakristalin, Fe lapisan tipis, dan Fe refraktori untuk memperhitungkan kemungkinan penggabungan Fe ke dalam melilit dan C 3 A. Temuan ini menekankan bahwa kompleksitas struktural dan morfologi katalis sintesis amonia multi-promosi teknis menembus semua skala panjang dari skala mikro (>1 µm), melalui skala nano (<100 nm) hingga ke tingkat atom.

Gambar 5
Buka di penampil gambar
Kekuatan Gambar
Memeriksa besi amonia pada skala atom: lapisan rangka Fe dengan lapisan tipis Fe dan Fe tahan api: a–c) Gambar HR-TEM yang direkam pada posisi berbeda dengan FFT (a) dan dari area yang disorot dalam (b) dan (c) yang ditunjukkan dalam sisipan dan penugasannya disajikan dalam Gambar S8 (Informasi Pendukung); d) Gambar STEM medan gelap dari lamela yang disiapkan FIB dan e,f) peta unsur yang direkam dari area yang dipilih dalam (d) menunjukkan distribusi Fe, Ca, dan O; Spektrum EELS dari tepi Fe L 2,3 -, O K- dan peta rasio intensitas garis putih L 3 -ke-L 2 dari Fe ditunjukkan dalam Gambar S9 (Informasi Pendukung).
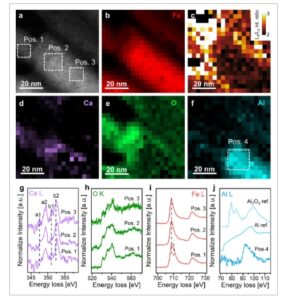
Sifat heteroatom yang terlarut dalam kisi Fe tidak dapat ditentukan hanya dengan pencitraan saja. Untuk lebih jauh mengeksplorasi kimia kerangka Fe, pencitraan STEM kembali dikombinasikan dengan analisis EELS dari daerah massal yang berasal dari lamela yang disiapkan oleh FIB ( Gambar 6 ; Gambar S10 , Informasi Pendukung). Pemetaan STEM-EELS dari tepi Fe L 2,3 -, Al L 2,3 -, O K-, dan Ca L 2,3 – masing-masing disajikan pada Gambar 6b–f . Pemetaan STEM-EELS dari tepi Fe L 2,3 – menunjukkan bahwa area terang di daerah minat (ROI) yang sesuai pada Gambar 6b kaya akan Fe. Selain itu, rasio intensitas garis putih L 3 -ke-L 2 dari tepi Fe L 2,3 – yang disajikan menyiratkan bahwa spesies Fe seperti logam hadir yang dapat ditemukan di area kanan bawah dan spesies Fe teroksidasi terletak di area tengah dan kiri atas daerah yang diselidiki. Selain itu, distribusi sinyal tepi O K menunjukkan distribusi oksigen yang tidak merata di wilayah ini, yang diperkaya di bagian kiri tengah (Pos.1 dan 2), tetapi terkuras di bagian kanan bawah area ini (Gambar 6e ).
Gambar 6
Buka di penampil gambar
Kekuatan Gambar
Studi unsur lokal kerangka Fe dengan STEM-EELS: a) Citra STEM lamela yang disiapkan FIB dan b,d–f) peta unsur tepi Fe L 2,3 -, Ca L 2,3 -, O K- dan Al L 2,3 – ; c) Peta rasio intensitas garis putih tepi Fe L 3 -ke-L 2 – ; g–i) Spektrum tepi Ca L 2,3 -, O K- dan Fe L 2,3 – yang diambil dari tiga area yang disorot dalam (a); j) Spektrum EELS tepi Al L 2,3 – yang direkam dari area yang disorot dalam (f); Gambaran umum citra STEM lamela yang disiapkan FIB ini ditunjukkan dalam Gambar S10 (Informasi Pendukung).
Spektrum tepi Ca L 2,3 menunjukkan perbedaan struktural promotor (Gambar 6d,g ). Intensitas puncak a1 dan b1 yang sesuai lebih jelas pada Pos. 2 dan 3, sementara fitur yang sama lebar dan datar pada Pos.1. Selain itu, rasio intensitas b2/a2 jauh lebih kecil pada Pos.1 dibandingkan dengan dua posisi lainnya. Ini menunjukkan bahwa koordinasi Ca 2+ lokal bervariasi. [ 44 , 45 ] Khususnya untuk Pos. 1, puncak b2 bergeser ke kehilangan energi yang lebih tinggi, yang konsisten dengan laporan sebelumnya untuk Ca 2+ yang berada dalam koordinasi kubik. [ 46 ] Ini sejalan dengan sedikit perubahan pada tepi O K (Gambar 6h ). Selain itu, tepi Fe L 2,3 (Gambar 6i) pada Pos. 2 dan 3 dicirikan oleh tepi Fe L 3 yang timbul pada 708 eV dan rasio intensitas garis putih L 3 -ke-L 2 sebesar 2,10, sementara bahu tambahan pada kehilangan energi yang lebih tinggi dari tepi Fe L 3 terjadi pada Pos. 1, yang mengindikasikan koeksistensi spesies Fe teroksidasi dan metalik di area ini.
Al diperkaya di bagian kanan bawah gambar dan hidup berdampingan dengan Fe seperti yang ditunjukkan oleh distribusi spasial tepi Al L 2,3 (Gambar 6f ). Namun, spektrum eksperimental tepi Al L 2,3 bersifat kompleks dan tidak mereproduksi Al 2 O 3 maupun spektrum referensi Al metalik (Gambar 6j ) karena pra-tepi karakteristik dan onset tertunda tidak ada. Satu kemungkinan interpretasi dari fitur unik ini adalah bahwa Al di wilayah yang disorot terkoordinasi secara tetrahedral, yang menghasilkan kehilangan intensitas pada ≈75–90 eV. [ 47 , 48 ] Lebih jauh, kami juga mempertimbangkan kemungkinan bahwa blok penyusun molekuler FeAl 2 O 4 /Al 2 O 3 dimasukkan ke dalam Fe yang memberikan kerangka Fe sifat parakristalin karakteristiknya. [ 26 , 49 ] Selain itu, analisis STEM-EDX pada permukaan dekat daerah menunjukkan bahwa nanopartikel Fe dapat berinteraksi dengan K dan didukung oleh oksida tahan api yang terdiri dari Ca, Al, K, dan O, yaitu, blok pembangun C 3 A (Gambar S11 , Informasi Pendukung). Munculnya nanopartikel Fe dapat mengubah aksesibilitas permukaan Fe dan dapat mengubah kinerja katalitik secara lokal.
3 Diskusi
Secara keseluruhan kontribusi ini menunjukkan bahwa katalis Haber Bosch teknis merupakan mahakarya mesoteknologi. Katalis ini merakit sendiri dari prekursor oksida selama aktivasi reduktif menjadi entitas berpori yang rumit dan hierarkis dengan sifat-sifat unik, di mana promotor memiliki peran multifungsi. Tingkat proses perakitan sendiri ditentukan oleh paket promotor, [ 33 ] potensi kimia dari kondisi aktivasi, dan seni sintesis prekursor untuk mengendalikan struktur prekursor yang stabil secara kinetik.
Kami selanjutnya mengungkap ketidakhomogenan struktural dan kompleksitas penjembatan skala dari katalis sintesis amonia teknis yang sesuai dengan fenomena multiskala yang dijelaskan oleh Alwin Mittasch. [ 50 ] Temuan kami mencakup identifikasi tipe struktur kristal C 3 A dan melilite sebagai fase tambahan dan setidaknya empat bentuk besi amonia yang berbeda. Secara khusus, C 3 A dan melilite belum pernah dilaporkan sebelumnya sebagai komponen dalam katalis sintesis amonia apa pun.
3.1 Tentang Struktur C3A
Bahan utama struktur C3A adalah cincin yang tersusun dari enam unit tetrahedral AlO4 yang berbagi sudut ( Gambar 7 a , b ; S12 , Informasi Pendukung) yang menggambarkan paralel dengan susunan tetrahedra SiO4 dalam silikat berlapis. [ 51 ] Cincin heksagonal tersebut disatukan oleh kation Ca2 + , yang menempati 72 dari 80 lubang yang mungkin. Secara umum, terdapat enam situs Ca yang berbeda dalam sel satuan, yang dibedakan oleh koordinasi (6 atau 8 kali lipat), distorsi polihedra, dan kekuatan ikatan Ca─O. Pemindahan informasi ini ke elemen-elemen yang terlibat dalam katalis multi-promosi teknis menunjukkan bahwa rumus jumlah kompleks teoritis yang mirip dengan K2x ( Ca, Fe) 3-xy [(Al,Fe) 1 -ySiy ] O6 mungkin dapat dilakukan dalam sistem katalis kami. [ 52 ] Namun, seperti yang ditunjukkan pada Tabel 1 , parameter kisi a dari C 3 A adalah 15,25 Å (prekursor) dan 15,27 Å (teraktivasi) dan dengan demikian, serupa dengan C 3 A murni (15,26 Å), yang menunjukkan hanya variasi komposisi yang sangat kecil dibandingkan dengan komposisi ideal.
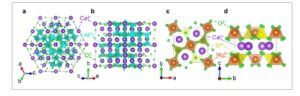
Gambar 7
Buka di penampil gambar
Kekuatan Gambar
Representasi struktur C 3 A dan tipe struktur melilite. a,b) Pandangan berbeda tentang struktur kristal C 3 A; c,d) Pandangan berbeda tentang tipe struktur melilite.
Karena sifat basanya yang tinggi, C 3 A digunakan sebagai pengeras kilat dalam kimia semen karena sejumlah kecil air dapat memulai hidrasi cepatnya, menghasilkan pengaturan awal semen dan dispersi domain alite dan belite. [ 53 ] Ini mirip dengan pengamatan kami, bahwa kristal wüstite disatukan oleh promotor yang menunjukkan bahwa C 3 A berkontribusi dengan sifat semennya. Kualitas ini juga dapat mencegah sistem dari disintegrasi selama aktivasi reduktif ketika perubahan struktural dan morfologi yang luar biasa terjadi karena transformasi seperti cangkang inti-retak dari wüstite menjadi α-Fe. [ 22 , 33 ] Selain itu, reaktivitasnya yang tinggi terhadap air, yang terbentuk setelah aktivasi reduktif, dapat menyebabkan hidrat yang membentuk platelet permukaan, yang dapat bertindak sebagai pendukung untuk nanopartikel Fe (Gambar S12 dan S13 , Informasi Pendukung). Penyerap air ini mungkin penting karena bahan baku sintesis amonia industri mengandung beberapa bagian per juta air dari proses steam reforming metana di hulu untuk menghasilkan H 2 . [ 54 ] Fitur unik C 3 A ini menjamin stabilitas karakteristik sistem katalis selama bertahun-tahun.
Selain itu, C3A adalah padatan yang tidak kongruen, menyiratkan bahwa bahan fase murni hanya dapat diperoleh ketika campuran stoikiometris dari unsur-unsur yang terlibat ditempa mendekati suhu dekomposisi termodinamikanya (1540 °C). Selama sintesis leburan prekursor, wüstite cair digunakan sebagai pelarut yang memungkinkan sintesis C3A dengan bantuan medium fluks. [ 55 ] Pemadatan wüstite memulai pemisahan fase yang menghasilkan struktur seperti batu bata yang khas (Gambar 3a ). Namun, karena difusi yang lambat selama pengerasan, sejumlah kecil heteroelemen akan tetap berada dalam fase wüstite yang memberikan sifat khas besi amonia. [ 31 ] Selain itu, aluminat juga dapat berkontribusi pada sintesis amonia dengan membentuk elektroda, yang bertindak sebagai donor elektron dan senyawa penyimpan hidrogen reversibel. [ 56 ] Fungsi tersebut dilaporkan dalam sistem katalis berbasis Rh yang membentuk struktur serupa seperti yang ditunjukkan pada Gambar S11 (Informasi Pendukung). [ 56 ]
3.2 Jenis Struktur Melilite
Tipe struktur melilite adalah larutan padat antara gehlenite kaya Al dan åkermanite kaya Mg. Silikat ini adalah senyawa berlapis yang terdiri dari lembaran yang tersusun dari tetrahedra berukuran berbeda dan kation Ca 2+ di interlayer (Gambar 7c,d ). [ 57 ] Dalam åkermanite, tetrahedron yang lebih kecil menggunakan kation Si 4+ (jari-jari ionik: 0,26 Å) sebagai elemen pusat, tetrahedron yang lebih besar dapat menampung kation dengan jari-jari yang lebih besar, misalnya Mg 2+ (jari-jari ionik: 0,57 Å) atau Fe 2+ (jari-jari ionik: 0,63 Å). [ 58 ] Dalam gehlenite, kation Mg 2+ dan sebagian kation Si 4+ disubstitusi secara isomorfik oleh kation Al 3+ (jari-jari ionik: 0,39 Å). [ 58 ] Oleh karena itu, ia merupakan salah satu dari sedikit oksida yang dapat menampung kation Mg 2+ dan Fe 2+ yang terkoordinasi empat kali lipat. [ 59 ] Di hadapan Fe 2+ , fase-fase ini dapat mengalami transisi fase tidak sepadan/sepadan pada suhu 250 °C, di mana di atasnya perpindahan kation dan diferensiasi situs tetrahedra menghilang. [ 59 ]
Mirip dengan C3A, melilite tidak hanya berfungsi sebagai semen struktur untuk memastikan stabilitas jangka panjang dari sistem katalis, tetapi juga merupakan larutan padat ideal yang mampu menampung berbagai macam elemen yang berbeda. Melilite yang ditemukan dalam prekursor dicirikan oleh perubahan anisotropik dari parameter kisi. Parameter kisi yang lebih kecil a ( a = 7,78 Å, prekursor; a = 7,77 Å, teraktivasi), tetapi parameter kisi yang lebih besar c ( c = 5,12 Å, prekursor dan teraktivasi) ditemukan dibandingkan dengan nilai nominal ( a = 7,84 Å, c = 5,01 Å dari åkermanite, Tabel 1 ). Ukuran bidang a,b dalam sel satuan terutama dipengaruhi oleh kation pada asal sel satuan (Gambar 7c ). Dengan demikian, substitusi isomorf parsial kation divalen dalam rongga tetrahedra yang lebih besar, misalnya, Fe 2+ atau Mg 2+ oleh kation bervalensi lebih tinggi, tetapi lebih kecil, misalnya kation Al 3+ , dapat menyebabkan penyusutan parameter kisi a . Ini akan menggeser larutan padat ke arah gehlenit. Hipotesis ini konsisten dengan pengamatan kami dalam data EELS (Gambar 6j ). Selain itu, ekspansi sepanjang sumbu c dapat dirasionalisasi dengan menambahkan kation yang lebih besar pada situs Ca 2+ , seperti K + . Ini dapat menghasilkan spesies K + mobil dalam kondisi reaksi. Dengan demikian, substitusi satu Mg 2+ /Fe 2+ dengan satu Al 3+ dan satu Ca 2+ dengan satu K + juga menjaga integritas muatan. Kehadiran kalium disarankan oleh Somorjai et al. untuk membuat situs aktif dan berpartisipasi dalam aktivasi N 2 . [ 60 , 61 ] Sebagai alternatif, situs Si 4+ juga dapat digantikan secara isomorfik oleh spesies Al 3+ .
Pada katalis yang diaktifkan, rasio melilite/C 3 A meningkat dari 1,7 menjadi 3,1 (Tabel 1 ). Perubahan ini tidak hanya menunjukkan bahwa tipe struktur melilite adalah senyawa yang stabil dalam kondisi reaksi, tetapi juga menunjukkan bahwa gibbsite dan bagian dari daerah amorf mungkin telah mengkristal menjadi tipe struktur melilite metastabil. [ 59 ] Parameter kisi tipe struktur melilite dalam katalis yang diaktifkan tetap tidak berubah dalam kesalahan pengukuran (Tabel 1 ), yang tampaknya menguatkan pembentukan gehlenite yang kaya Al 3+ . Namun, jika setiap Al 3+ dari gibbsite telah dimasukkan ke dalam fase gehlenite yang baru terbentuk, strukturnya akan sangat terkuras dalam kation Si 4+ yang lebih besar untuk menjaga netralitas muatan. Ini adalah skenario yang sangat tidak mungkin. Jadi, seperti yang disarankan oleh studi mikroskopi kami (Gambar 6 ; Gambar S11 , Informasi Pendukung), aluminium juga dapat larut dalam fase lain, termasuk fase Fe.
Selain itu, percobaan spektroskopi fotoelektron sinar-X tekanan sekitar (NAP-XPS) memberikan bukti kuat untuk melilite stabil dan fase promotor semen C 3 A selama sintesis amonia (Gambar S13 , Informasi Pendukung). Pada 540 °C, spektrum tingkat inti Ca 2p, Al 2p, dan Si 2p menunjukkan fitur yang dapat dikaitkan dengan kalsium silikat atau silikoaluminat dan aluminat. [ 62 – 64 ] Fase semen stabil ini dapat secara efektif menyatukan butiran besi dan berfungsi sebagai sistem penyangga untuk memasok integrasi heteroelemen ke dalam besi amonia, sehingga mempertahankan regangan kisi dan sifat parakristalin dalam kondisi reaksi. Jenis struktur melilite mungkin juga ada dalam percobaan sintesis amonia awal yang dilakukan oleh Fritz Haber. Asbes krisotil (Mg,Fe,Ni) 3 Si 2 O 5 (OH) 4 telah digunakan sebagai pendukung untuk bahan aktif. Dalam penelitian ini, sintesis amonia dilakukan hingga suhu 1100 °C. [ 65 ] Pada suhu ini, material krisotil terurai menjadi diopside, melilit, dan forsterit. [ 66 ] Selain itu, sebagian besi dapat dilepaskan dari struktur selama proses dekomposisi yang mengarah ke sistem katalis logam yang didukung atau ke koeksistensi Fe logam dan teroksidasi dalam jarak dekat yang mirip dengan temuan yang disajikan pada Gambar 5 dan 6 dan Gambar S11 (Informasi Pendukung). [ 67 ]
3.3 Tentang Struktur Besi Amonia
Besi amonia merangkum karakter khusus besi yang digunakan dalam sintesis amonia dibandingkan dengan α-Fe murni. [ 68 ] Telah ditekankan bahwa besi amonia tersusun atas lapisan-lapisan, [ 22 ] memperlihatkan regangan [ 31 ] atau memperlihatkan karakteristik parakristal, [ 26 ] di mana inklusi molekuler Al x O y mengganggu kisi inang α-Fe. Studi kami memperluas perspektif ini dengan memperkenalkan integritas besi amonia di seluruh skala panjang, mengungkap pluralisme dan kompleksitas struktural yang belum pernah terjadi sebelumnya dalam katalis sintesis amonia teknis yang dipromosikan secara ganda ( Gambar 8 ; Tabel S2 , Informasi Pendukung). Telah ditunjukkan sebelumnya bahwa kisi Fe yang tegang penting untuk kinerja optimal katalis sintesis amonia. [ 69 , 70 ] Regangan memodifikasi jarak atom secara lokal dan menyebabkan permukaan berundak. [ 71 – 73 ] Permukaan berundak penting untuk aktivasi N 2 . [ 74 , 75 ] Literatur baru-baru ini juga menyoroti bahwa besi amonia berfungsi sebagai prototipe parakristal. [ 26 , 49 ] Parakristalinitas tersebut berasal dari penggabungan Al ke dalam kisi Fe, yang secara efektif mempertahankan luas permukaan tinggi katalis Haber Bosch dan, dengan demikian, berkontribusi pada stabilitas jangka panjang yang luar biasa dari katalis ini. [ 76 , 77 ]

Gambar 8
Buka di penampil gambar
Kekuatan Gambar
Skema yang merangkum keluarga besi amonia dan fase promotor semen beserta fungsi yang diharapkan pada skala yang berbeda. Karakter miring dan tebal mewakili struktur yang baru ditemukan dalam katalis Haber Bosch. Rincian lebih lanjut dapat ditemukan di Tabel S2 (Informasi Pendukung).
Selain itu, pada deskripsi besi amonia yang diketahui, perimeter platelet-Fe, rangka Fe, lapisan tipis Fe, dan Fe refraktori telah diidentifikasi sebagai konstituen baru dari keluarga besi amonia, yang tampaknya ada dalam keadaan metastabil yang sangat adaptif terhadap kondisi reaksi. Seperti yang ditunjukkan oleh analisis HR-TEM kami (Gambar 5 ), perubahan dalam parameter kisi mungkin kecil, tetapi perubahan tersebut sudah dapat menjadi penting untuk membentuk besi amonia aktif.
Penting untuk dicatat bahwa bidang kisi (110) sebagian besar telah diidentifikasi dalam sistem katalis ini. Dalam pekerjaan sebelumnya pada sistem model Fe, permukaan (111) menunjukkan laju tertinggi untuk disosiasi N 2 , sementara laju rendah untuk permukaan (110). [ 12 , 78 ] Namun, ditunjukkan oleh Somorjai et al. bahwa dengan adanya promotor, permukaan tersebut dapat diubah menjadi sistem aktif untuk sintesis amonia, yang membuka jalan bagi pentingnya mempertimbangkan kompleksitas dalam katalisis heterogen. [ 79 ] Kami menyoroti bahwa temuan yang dijelaskan dalam manuskrip ini tidak bertentangan dengan wawasan skala atomistik sebelumnya dari teori dan eksperimen, sebaliknya, kami memperluasnya ke dimensionalitas dan kompleksitas yang lebih tinggi.
Untuk desain katalis yang rasional, gambaran holistik dari struktur diperlukan karena semua konstituen besi amonia harus memenuhi tugas masing-masing pada waktu tertentu selama sintesis amonia. Jika skala waktu dari tugas yang berbeda tidak cocok atau prosesnya tidak berkelanjutan, katalis akan dinonaktifkan. Hal ini ditunjukkan secara mengesankan oleh pemilihan fase promotor kristal. Oksida-oksida ini harus cukup basa untuk mendorong desorpsi amonia, tetapi pada saat yang sama, oksida-oksida ini harus inert dan tidak bereaksi dengan NH3 dalam kondisi autogen karena oksida-oksida ini secara bersamaan harus menstabilkan struktur. Selain itu, interaksi rumit dari berbagai konstituen besi amonia yang dipasangkan dengan pluralisme struktural dan komposisi membangun struktur katalitik aktif berpori hierarkis, di mana beberapa situs aktif yang berbeda dapat hidup berdampingan dan dapat membentuk amonia melalui berbagai jalur yang diatur dan disinkronkan oleh potensi kimia lokal. Studi operando yang lebih rinci diperlukan untuk lebih mendukung hipotesis ini.
Selain itu, dalam wilayah film tipis, Fe terdistorsi hidup berdampingan dengan Fe refraktori yang dimasukkan ke dalam tipe struktur melilite dan C3A yang menunjukkan bahwa spesies Fe2 + kationik tidak dapat dikecualikan dalam sistem katalis aktif dalam kondisi reaksi. Faktanya, telah disarankan dari studi Mößbauer sebelumnya bahwa sekitar 1 wt.% besi hadir sebagai spesies ferrous. [ 29 ] Selain itu, struktur ini, termasuk film tipis dan cangkang promotor yang menutupi kerangka Fe (Gambar 5 dan 6 ) dapat menstabilkan katalis teknis multi-promosi dari sintering dan memoderasi pasokan heteroelemen dalam fase α-Fe massal untuk mengimbangi kemungkinan penipisan heteroelemen selama reaksi dari fase aktif. Ini juga sejalan dengan studi sebelumnya yang menunjukkan bahwa lapisan tipis alumina menutupi partikel besi dan mencegah sintering. [ 29 ] Heteroelemen dalam α-Fe penting karena dapat menimbulkan tekanan pada permukaan, yang mengakibatkan disosiasi nitrogen lebih mudah, [ 80 , 81 ] mengatur kinetika dinamika permukaan [ 82 – 84 ] dan mengubah α-Fe yang kurang aktif menjadi material yang sangat aktif untuk sintesis amonia. [ 85 ] Dengan cara ini, umur pakai yang panjang hingga 10 tahun dapat dijelaskan dan aktivitasnya dapat terus diregenerasi.
Di sisi lain, situs C7 besi secara luas dianggap sebagai pusat aktif untuk sintesis amonia. Kami berspekulasi bahwa, dalam konteks ini, pusat C7 dapat semakin terbentuk pada lapisan besi 2D yang diperluas, dan distribusi spasial dan temporal mereka pada lapisan ini dijamin oleh umpan balik dengan potensi kimia lokal. [ 86 ] Ini akan menciptakan situasi yang menyerupai transisi fase frustrasi antara Fe metalik dan Fe-N, menghasilkan sistem dinamis di mana siklus katalis dapat ditutup secara rata-rata. [ 87 ] Jika transisi fase ke pembentukan nitrida selesai, dinamika spasiotemporal ini tidak lagi mungkin dan penonaktifan terjadi.
4 Kesimpulan
Singkatnya, kami menggambarkan struktur mesoskopik katalis sintesis amonia teknis dan mengidentifikasi integritas struktural besi amonia di berbagai skala panjang menggunakan pendekatan karakterisasi multimoda berdasarkan difraksi, spektroskopi, dan mikroskopi. Sistem katalis dicirikan oleh heterogenitas komposisi dan morfologi intrinsik serta kompleksitas yang belum pernah dipertimbangkan sebelumnya dalam pemodelan teoritis dan melibatkan permukaan luar serta bagian berpori. Kami menemukan dua struktur tambahan, yaitu C 3 A dan tipe struktur melilite yang mungkin memainkan peran penting dalam seluruh proses sintesis amonia sebagai penyangga elektroda, agen penstabil terhadap sintering, pasokan heteroelemen, penyerap air atau semen struktural untuk mencegah disintegrasi domain besi selama aktivasi. Secara total, kami mengidentifikasi empat struktur besi tambahan yang harus dimasukkan ke dalam keluarga struktur besi amonia yang ada, yaitu perimeter platelet-Fe, kerangka Fe, lapisan tipis Fe, dan Fe refraktori. Pluralisme struktural yang diamati menunjukkan bahwa beberapa situs aktif dengan jalur reaksi yang berbeda dapat hidup berdampingan dalam katalis ini. Kinerja yang berlaku dapat ditentukan oleh potensi kimia lokal dan dapat bervariasi di seluruh struktur katalis lokal. Reaktivitas lokal ini juga dapat melibatkan distribusi spasial dan temporal dari situs C7 yang aktif dan dinamis, yang memungkinkan pembangkitan, konsumsi, dan regenerasi yang efisien. Dengan demikian, studi ini menyoroti tantangan yang muncul seiring dengan pengoptimalan sistem katalis ini dan pemahaman sifat di baliknya. Terakhir, studi ini memberikan momentum baru untuk melakukan studi operando terperinci dan pengembangan strategi sintetis untuk desain katalis rasional menuju katalis berkinerja tinggi yang baru.
5 Bagian Eksperimen
Sintesis Prekursor Katalis
Prekursor katalis teknis multi-promoted disiapkan dalam tanur busur listrik mengikuti resep dan skala yang relevan untuk aplikasi industri. Bahan baku dicampur bersama sebagai bubuk halus, dan campuran tersebut ditempatkan di dalam panci peleburan skala industri. Tegangan diberikan, menciptakan busur listrik. Ketika proses peleburan selesai, lelehan dipadamkan dan padatan dihancurkan.
Sintesis Amonia
Sampel katalis yang diaktifkan setelah pengujian aktivitas selama 96 jam dibuat dalam set-up aliran baja tahan karat komersial (Integrated Lab Solutions Gmbh) yang dilengkapi dengan reaktor pelindung, reaktor sintesis, dan detektor IR on-line untuk NH 3 dan H 2 O (Emerson X-stream) untuk analisis gas produk kuantitatif. Untuk deskripsi terperinci tentang set-up tersebut, lihat referensi. [ 88 ]
Untuk menyiapkan lapisan katalis, 3 g prekursor katalis berbasis Fe (fraksi partikel 425–560 µm) diencerkan dengan 3,9 g SiC (ukuran partikel rata-rata 154 µm). Lapisan katalis ditempatkan dalam reaktor sintesis di antara SiC murni dan posisinya ditetapkan oleh sumbat wol kuarsa di pintu masuk dan pembuangan reaktor. Setelah pembersihan reaktor secara intensif hingga kadar air stabil pada hampir nol, sampel diaktifkan mengikuti petunjuk produsen katalis dengan memanaskannya dalam aliran gas 858 NmL min −1 (75% H 2 , 25% N 2 ) dengan suhu meningkat hingga 500 °C pada tekanan tinggi 90 bar(g). Prekursor direduksi dalam tiga langkah suhu dengan laju pemanasan yang berbeda: dari suhu ruangan hingga 250 °C dengan 1,2 °C min -1 , 250–400 °C dengan 0,3 °C min -1 dan 400–500 °C dengan 0,2 °C min -1 . Setelah itu, kondisi dipertahankan konstan selama 4,5 jam. Secara total, prosedur reduksi memakan waktu 24 jam.
Selanjutnya dilakukan uji aktivitas dengan menurunkan laju alir total menjadi 357 NmL min -1 (75% H 2 , 25% N 2 ) dan mengikuti program temperatur sambil mempertahankan tekanan 90 bar(g). Pada program temperatur tersebut, unggun katalis dipertahankan pada suhu 500 °C selama 2 jam pertama kemudian didinginkan hingga suhu 400 °C pada laju 1 °C min -1 . Secara total, uji aktivitas isotermal pada suhu 400 °C dan pendinginan sebelumnya berlangsung selama 22 jam. Selanjutnya, unggun katalis dipanaskan kembali pada suhu 1 °C min -1 hingga mencapai suhu 500 °C. Uji aktivitas isotermal pada suhu 500 °C dan pemanasan sebelumnya tersebut berlangsung total selama 14 jam. Setelah peningkatan ini dilakukan dua kali, lapisan katalis didinginkan hingga 400 °C pada laju 1 °C min −1 . Suhu ini dipertahankan hingga durasi total uji aktivitas tercapai selama 96 jam. Pada akhir pengukuran, tekanan dilepaskan dan lapisan katalis didinginkan hingga suhu ruangan dan dibilas dengan nitrogen. Aktivitas sintesis amonia selama 96 jam ini diilustrasikan dalam Gambar S2 (Informasi Pendukung).
Akhirnya, katalis yang telah diaktifkan dipindahkan ke glovebox dan disimpan di sana tanpa terkena udara. Kinerja katalis ini sebelumnya telah dipublikasikan dalam referensi. [ 33 ]
Difraksi Sinar-X (XRD)
Pengukuran XRD dilakukan dalam geometri Bragg-Brentano pada difraktometer theta/theta Bruker AXS D8 Advance A25, menggunakan radiasi Cu Kα 1+2 dan detektor strip silikon LynxEye XE-T dispersif energi yang peka terhadap posisi dalam mode resolusi energi tinggi (tidak memerlukan filter Kβ). Dalam kasus katalis bekas yang dipasivasi, pengukuran tambahan dengan pengaturan yang sama dilakukan dengan radiasi Mo Kα 1+2 untuk mengakses refleksi orde lebih tinggi. Serbuk sampel diisi ke dalam rongga tempat sampel kristal tunggal silikon dengan latar belakang rendah, permukaan tempat serbuk sejajar dengan tepi tempat sampel (pemuatan depan). Prakatalis wüstite FeO digiling dengan hati-hati dan diukur dengan rotasi sampel untuk meningkatkan statistik penghitungan. Awalnya, sampel bekas dikarakterisasi dalam tempat sampel kedap udara dengan tutup berbentuk kubah. Namun, karena latar belakang yang tinggi dan noise yang sesuai yang disebabkan oleh kubah polimer, sensitivitas pengukuran tidak cukup untuk mendeteksi fase minoritas. Oleh karena itu, tutup tempat sampel dilonggarkan sedikit untuk secara sengaja membocorkan oksigen ke tempat sampel semalaman, sehingga katalis yang tereduksi menjadi pasif. Setelah pasifasi berhasil, katalis bekas digiling ulang dan dikarakterisasi dengan rotasi sampel, menggunakan radiasi Cu dan Mo. Semua pola XRD direkam dalam mode pemindaian berkelanjutan dalam kisaran 5–135° 2θ dengan penambahan 0,02° dan waktu penghitungan 1 detik per langkah, sehingga menghasilkan total waktu akumulasi 192 detik per titik data.
Identifikasi fase dilakukan menggunakan DIFFRAC.EVA (v6, 2010–2021 Bruker AXS) yang dikombinasikan dengan basis data ICDD PDF-4+. Untuk analisis Rietveld, digunakan DIFFRAC.TOPAS (v5, 1999–2014 Bruker AXS). Model struktur kristal untuk fase sekunder diambil dari basis data ICSD. Meskipun fase tipe melilite dan kalsium trialuminate yang diamati kemungkinan merupakan larutan padat yang mengandung unsur-unsur tambahan, seperti yang ditunjukkan oleh parameter kisi yang menyimpang dan intensitas relatifnya, tidak ada upaya yang dilakukan untuk menyempurnakan model struktur fase minoritas. Refleksi wüstite dalam prakatalis menunjukkan profil puncak yang sangat asimetris dengan ekor di sisi sudut yang lebih tinggi, yang menunjukkan distribusi yang luas dalam ukuran domain kristalit dan parameter kisi. Oleh karena itu, pola tersebut didekati dalam kecocokan Rietveld menggunakan dua fase tipe wüstite. Namun, pendekatan ini tidak dimaksudkan untuk menyiratkan keberadaan sebenarnya dari dua fase wüstite yang terpisah, tetapi lebih digunakan sebagai solusi untuk menangani distribusi kontinu dalam kemungkinan terbatas dari metode Rietveld. Karena parameter kisi wüstite variabel terutama terkait dengan stoikiometri cacat kation Fe 1− x O, rumus x = 1-( a [Å]-3,856)/0,478 digunakan untuk memperkirakan nilai perkiraan x yang sesuai dengan masing-masing “fase” wüstite. [ 89 ]
Mikroskop Elektron Pemindaian (SEM)
Pengukuran SEM dilakukan pada mikroskop Hitachi S-4800 yang dilengkapi dengan pistol emisi medan dingin. Selama pengukuran, tegangan percepatan 1,5 kV dan jarak kerja 4 mm dipilih untuk mengambil gambar. Pemetaan unsur EDX dilakukan pada tegangan percepatan 15 kV dan jarak kerja 10 mm menggunakan spektrometer QUANTAX 800 EDX dispersif energi dan detektor XFlash 6–30. Selain itu, katalis yang diaktifkan dipindahkan dari reaktor ke dalam glovebox dan selanjutnya dipasang pada dudukan sampel inert Al. Dudukan inert dipasang di ruang pertukaran gas SEM untuk memastikan sampel tidak terpapar udara selama prosedur ini.
Sinar Ion Terfokus (FIB)
Lamella dari prekursor dan katalis yang diaktifkan disiapkan dengan metode FIB, menggunakan sistem ThermoFisher Helios NanoLab G3 FIB-SEM DualBeam. Secara khusus, ion Galium digunakan dengan energi hingga 30 keV. Posisi pemotongan lamella dipilih untuk mencakup sebanyak mungkin morfologi yang berbeda guna memperoleh informasi yang maksimal. Perhatian khusus telah diberikan untuk meminimalkan kerusakan dan pengendapan ulang material yang dihilangkan, menggunakan energi ion rendah (5 dan 2 keV) selama langkah pemolesan akhir. Katalis yang diaktifkan dipindahkan secara inert dari kotak sarung tangan ke mikroskop dan kembali.
Mikroskop Elektron Transmisi
Untuk analisis TEM, digunakan JEOL JEM-ARM 200F pada tegangan operasi 200 kV. TEM ini dilengkapi dengan cold FEG (field-emission electron gun), korektor C s untuk aberasi sferis untuk mode TEM dan STEM, kamera Gatan Oneview dan Orius untuk memperoleh gambar TEM, detektor medan terang dan medan gelap annular untuk mengumpulkan gambar STEM serta spektrometer EDX dan EEL untuk analisis unsur. Sedangkan untuk katalis yang diaktifkan dan yang sudah habis, pemindahan lamela FIB dari glovebox ke TEM dilakukan dengan menggunakan vacuum transfer holder tanpa oksigen. Selain itu, digunakan mikroskop FEI/TFS Talos F200X yang dioperasikan pada 200 kV, yang dilengkapi dengan detektor Super X EDX.
Spektroskopi Penyerapan Sinar-X (XAS)
Penyerapan sinar-X di dekat struktur tepi (XANES) diperoleh dari pengukuran XAS ex situ pada tepi K Fe (7112 eV) yang dilakukan dalam mode transmisi pada garis sinar CLAESS dari sinkrotron ALBA (Barcelona, Spanyol). Monokromator Si(111) digunakan untuk pemilihan energi. Cermin kolimasi vertikal dengan lapisan Si dan cermin pemfokus dengan lapisan Rh digunakan. Intensitas sinar-X sebelum dan sesudah sampel dipantau menggunakan ruang ionisasi yang diisi dengan campuran He dan N 2 56:44 (ruang I 0 ) atau campuran Kr dan N 2 9:91 (ruang I 1 ). Sampel disiapkan dengan mengencerkan katalis dengan boron nitrida dan menekan menjadi pelet. Sebelum dicampur dengan BN, katalis dihancurkan dan diayak dengan bukaan saringan 20 µm untuk meningkatkan homogenitas sampel.

