
Abstrak
Semikonduktor oksida logam (MOS) yang didukung material Pd merupakan kandidat potensial untuk sensor H 2 , sementara deteksi H 2 yang efektif pada suhu mendekati suhu kamar tetap menjadi tantangan besar karena sulitnya migrasi hidrogen dari Pd pada suhu rendah. Di sini, dipandu oleh perhitungan teoritis, atom tunggal tanah jarang yang mendoping nanopartikel Pd yang didukung pada nanorod WO 3 dengan perbedaan fungsi kerja yang dapat disetel (ΔФ) dan kekosongan oksigen dikembangkan secara tepat untuk meningkatkan kinerja penginderaan H 2 . Ce-Pd/WO 3 yang dihasilkan menyajikan respons tertinggi 31,3 terhadap 50 ppm H 2 , menunjukkan peningkatan 6 kali lipat dibandingkan Pd/WO 3 , yang mewujudkan jejak dan deteksi cepat H 2 . Hasil teori fungsi kerapatan mengungkapkan bahwa penghalang energi migrasi hidrogen dan energi pembentukan kekosongan oksigen berkurang setelah memperkenalkan atom tunggal tanah jarang, dan Ce-Pd/WO 3 dengan ΔФ terendah menunjukkan luapan dan desorpsi hidrogen yang paling mudah. Karakterisasi spektrum in situ dan eksperimen spillover hidrogen selanjutnya menunjukkan migrasi hidrogen yang sangat baik melalui Ce-Pd/WO 3 . Yang penting, aplikasi pemantauan waktu nyata perangkat Ce-Pd/WO 3 untuk kebocoran hidrogen (0,1 V/V%) dalam baterai Al-air juga diverifikasi. Pekerjaan ini dapat menjelaskan pengembangan sensor H 2 efisiensi tinggi melalui modulasi fungsi kerja yang tepat.
1 Pendahuluan
Sebagai sumber energi bersih dan terbarukan, hidrogen (H₂) sangat penting untuk mewujudkan tujuan puncak karbon dan netralitas karbon. [ 1 ] Namun, sifatnya yang sangat eksplosif telah menimbulkan masalah keamanan yang signifikan. [ 2 ] Oleh karena itu, mengembangkan sensor gas yang sangat sensitif untuk pemantauan jejak H 2 yang cepat dan akurat penting untuk aplikasinya yang aman. [ 3 ] Dibandingkan dengan sensor katalitik, konduktivitas termal, elektrokimia, dan regangan, sensor gas resistansi telah menarik perhatian yang cukup besar karena strukturnya yang lebih sederhana dan konsumsi daya yang lebih rendah. [ 4 ] Sensor H 2 resistif dapat dikategorikan menjadi dua jenis: sensor gas berbasis semikonduktor dan sensor gas berbasis logam. [ 5 ] Di antara mereka, bahan berbasis paladium (Pd) banyak digunakan untuk fabrikasi sensor H 2 canggih . [ 6 ] Meskipun demikian, aplikasi praktis bahan Pd tunggal untuk sensor H 2 terhambat karena: i) pembentukan PdH x selalu mengubah volume Pd, yang menyebabkan kinerja penginderaan tidak stabil, ii) afinitas H 2 yang kuat pada Pd membatasi desorpsi H, sehingga menghasilkan respons yang tidak memuaskan ( Gambar 1a , kiri). [ 7 ]
Gambar 1
Buka di penampil gambar
Presentasi PowerPoint
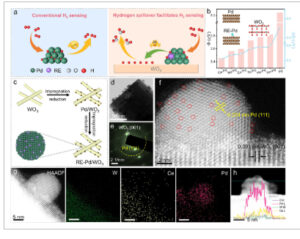
Prediksi teoritis, sintesis, dan karakterisasi RE-Pd/WO 3 . a) Ilustrasi skema penginderaan hidrogen konvensional pada Pd dan luapan hidrogen memfasilitasi penginderaan hidrogen pada RE-Pd/WO 3 . b) Fungsi kerja, perbedaan fungsi kerja untuk Pd, RE-Pd, Pd-WO 3 , dan RE-Pd/WO 3 . c) Diagram skema rute sintesis RE-Pd/WO 3 . d) Gambar HRTEM. e) Pola SAED yang sesuai. f) Gambar AC-TEM. g) Gambar pemetaan elemen EDS yang sesuai dari Ce-Pd/WO 3 . h) Pemindaian garis STEM-EDS dari Ce-Pd/WO 3 .
Mendukung Pd pada semikonduktor oksida logam (Pd/MOS) adalah pendekatan yang efektif untuk meringankan penyisipan H dalam Pd. Namun, adsorpsi hidrogen yang kuat menghambat spillover hidrogen dari Pd ke MOS, yang dapat secara serius membatasi proses penginderaan. [ 2 ] Hingga saat ini, banyak strategi, termasuk modulasi morfologi, [ 8 ] paduan, [ 7 , 9 ] dan konstruksi heterostruktur, [ 10 ] dll. telah dikembangkan untuk memodulasi spillover hidrogen untuk meningkatkan kinerja penginderaan H 2 . Misalnya, nanocavity penyangga Pd-NiO/SnO 2 kulit kuning telur dibangun untuk deteksi H 2 . Lapisan nanocavity berongga menyediakan situs aktif yang cukup untuk meningkatkan adsorpsi H 2 dan secara kinetik meningkatkan spillover hidrogen dari Pd ke dukungan, meningkatkan kinerja penginderaan hidrogen pada 230 °C. [ 11 ] Pada paduan PdCu yang didukung nanowire W 18 O 49 , keberadaan Cu memengaruhi struktur elektronik Pd, menghasilkan desorpsi hidrogen yang cepat dan pembentukan spesies oksigen, sehingga mewujudkan deteksi H 2 yang cepat pada suhu 125 °C. [ 12 ] Heterostruktur pada Pd-SnS 2 /SnO 2 memperluas lapisan deplesi elektron (EDL), yang mengarah pada peningkatan respons hidrogen pada suhu kerja yang tinggi. [ 13 ] Meskipun berbagai upaya telah dilakukan, pengembangan sensor efisiensi tinggi untuk deteksi H 2 pada suhu mendekati suhu ruangan masih menjadi tantangan besar karena masalah yang tertunda dari kesulitan migrasi H pada suhu rendah. [ 7 , 14 ] Dalam bidang elektrokatalitik, penelitian menunjukkan bahwa modulasi perbedaan fungsi kerja (ΔФ) dari Pd dan pendukung dapat memfasilitasi luapan hidrogen pada Pd. [ 15 ] Mengurangi ΔФ melalui penambahan kekosongan dapat meningkatkan desorpsi H, sehingga meningkatkan kinerja katalitik. [ 16 ] Lebih jauh lagi, ΔФ yang dioptimalkan dapat meningkatkan adsorpsi H dan mempercepat desorpsi H, yang selanjutnya meningkatkan aktivitas katalitik evolusi hidrogen. [ 17 ] Oleh karena itu, rekayasa ΔФ merupakan strategi yang efektif untuk mendorong migrasi H dari situs aktif ke situs pendukung. [ 15 , 18 ]Akan tetapi, sedikit penelitian yang berfokus pada modulasi ΔФ secara tepat untuk mengendalikan luapan H secara efisien guna mencapai jejak dan deteksi H₂ yang cepat pada suhu mendekati suhu ruangan.
Dibandingkan dengan logam transisi 3d, tanah jarang (RE) dapat digunakan untuk memodulasi struktur elektronik Pd secara tepat dan berkesinambungan karena pengisian nomor elektron 4f yang tidak lengkap. [ 19 ] Di sini, atom tunggal RE yang mendoping nanopartikel Pd yang didukung pada nanorod WO 3 (RE-Pd/WO 3 ) disintesis untuk sensor H 2 yang cepat dan sensitifitas tinggi pada suhu mendekati suhu kamar. Fungsi kerja Pd dapat dimodulasi secara tepat dengan mendoping atom RE (Ce, Nd, Eu, Tb, Ho, dan Tm), akibatnya, ΔФ menurun dalam RE-Pd/WO 3 dibandingkan dengan Pd/WO 3 . Selain itu, ΔФ meningkat dengan peningkatan nomor elektron orbital 4f dalam RE, dan konsentrasi kekosongan oksigen menunjukkan tren yang berlawanan dengan ΔФ. Ce-Pd/WO 3 dengan ΔФ terendah menyajikan properti penginderaan H 2 terbaik pada suhu mendekati ruangan. Perhitungan teori fungsi densitas (DFT) mengungkapkan bahwa ΔФ terendah mengarahkan penghalang energi luapan hidrogen terendah, sedangkan energi pembentukan kekosongan oksigen terendah memicu konsentrasi spesies oksigen (O 2 − ) tertinggi, yang memberikan Ce-Pd/WO 3 sensitivitas tertinggi dan waktu respons-pemulihan terpendek pada suhu mendekati ruangan, mengungguli sensor H 2 yang paling banyak dilaporkan . Luapan hidrogen yang ditingkatkan pada Ce-Pd/WO 3 selanjutnya dikonfirmasi oleh karakterisasi in situ dan eksperimen luapan hidrogen. Yang mengesankan, respons cepat terhadap kebocoran hidrogen pada baterai Al-air memverifikasi potensi aplikasi perangkat Ce-Pd/WO 3 pada suhu mendekati ruangan.
2 Hasil dan Pembahasan
Untuk mengatasi tantangan desorpsi hidrogen yang sulit pada sensor logam Pd tradisional, atom tunggal RE yang mendoping Pd yang didukung pada WO3 dirancang untuk memfasilitasi luapan hidrogen (Gambar 1a ). Model WO3 , Pd/ WO3 , dan RE-Pd/WO3 dibangun , dan fungsi kerja dihitung melalui DFT (Gambar S1–S8 , Informasi Pendukung). Seperti yang ditunjukkan pada Gambar 1b dan Tabel S1 (Informasi Pendukung), fungsi kerja Pd menurun dari 5,24 menjadi 3,46 (Ce-Pd), 3,56 (Nd-Pd), 3,59 (Eu-Pd), 3,73 (Tb-Pd), 3,78 (Ho-Pd), dan 3,82 eV (Tm-Pd). Dengan demikian, ΔФ (ΔФ = Ф RE-Pd –Ф WO3 ) antara RE-Pd dan WO 3 dihitung lebih lanjut. Dapat dilihat pada Gambar 1b dan Tabel S2 (Informasi Pendukung) bahwa ΔФ berkurang dari 2,23 (Pd/WO 3 ) menjadi 0,44 (Ce-Pd/WO 3 ), 0,55 (Nd-Pd/WO 3 ), 0,58 (Eu-Pd/WO 3 ), 0,71 (Tb-Pd/WO 3 ), 0,76 (Ho-Pd/WO 3 ), dan 0,80 eV (Tm-Pd/WO 3 ). Hasil ini memperkirakan bahwa mendoping RE ke dalam Pd merupakan cara efektif untuk memodulasi ΔФ, yang dapat meningkatkan luapan hidrogen melalui RE-Pd/WO 3 , sehingga meningkatkan kinerja penginderaan H 2 .
Nanopartikel Pd terdoping atom tunggal RE yang ditopang pada nanorod WO3 dirancang berdasarkan hasil perhitungan teoritis. Nanorod WO3 disintesis melalui metode hidrotermal, dan selanjutnya menggabungkan Pd dan RE ke dalam nanorod WO3 melalui impregnasi dan reduksi (Gambar 1c ). Hasil mikroskop elektron pemindaian (SEM) mengungkap struktur seperti batang 1D yang seragam dari WO3 , dengan panjang rata-rata ≈1,5 µm, lebar rata-rata ≈200 nm, dan rasio aspek 7:1 (Gambar S9 , Informasi Pendukung). Struktur nanorod terpelihara dengan baik dalam Ce-Pd/WO3 setelah kalsinasi. Gambar mikroskop elektron transmisi (HRTEM) resolusi tinggi dari Ce-Pd/WO3 selanjutnya memverifikasi struktur nanorod, dan nanopartikel Pd tersebar secara seragam pada nanorod WO3 dengan ukuran rata-rata ≈12,3 nm (Gambar 1d ; Gambar S10 , Informasi Pendukung). Pola difraksi elektron area terpilih (SAED) dari Ce-Pd/WO3 mengungkapkan bahwa faset kristal (001) dari WO3 dan faset kristal (111) dari Pd (Gambar 1e ), mengonfirmasi keberhasilan modifikasi nanopartikel Pd pada nanorod WO3 . Atom tunggal Ce yang terisolasi yang ditunjukkan oleh titik terang didoping pada kisi Pd dalam gambar mikroskop elektron transmisi (AC-TEM) yang dikoreksi aberasi sferis (Gambar 1f dan Gambar S14 , Informasi Pendukung), menunjukkan keberhasilan doping atom tunggal Ce dalam nanopartikel Pd. Sementara itu, jarak kisi yang jelas sebesar 0,391 dan 0,224 nm diamati pada Gambar 1f , yang sesuai dengan bidang (001) WO3 dan bidang (111) Pd, masing-masing, konsisten dengan hasil SAED. Distribusi unsur W, O, Ce, dan Pd dalam nanorod Ce-Pd/WO3 selanjutnya diperkuat oleh spektroskopi sinar-X dispersif energi yang sesuai (EDS, Gambar 1g ; Gambar S15 , Informasi Pendukung). Lebih jauh, pemindaian garis STEM-EDS melintasi partikel tunggal menunjukkan bahwa kandungan Ce lebih tinggi daripada W, yang menunjukkan titik terang pada nanopartikel Pd dikaitkan dengan atom tunggal Ce (Gambar 1h ).
Hasil spektrometer emisi optik plasma yang diinduksi (ICP-OES) menunjukkan bahwa kandungan Pd adalah 3,1 wt.% dan 3,2 wt.% dalam Ce-Pd/WO 3 dan Pd/WO 3 , masing-masing, dan kandungan Ce adalah 1,2 wt.% (Tabel S3 , Informasi Pendukung). Doping RE lainnya Pd/WO 3 dapat disintesis dengan mengganti hidrat cerium (III) asetat dengan garam tanah jarang lainnya melalui metode sintesis yang sama. Hasil SEM menunjukkan struktur nanorod dari semua sampel yang disiapkan, dan nanopartikel Pd tersebar secara merata pada nanorod (Gambar S11 , Informasi Pendukung, 13, 16, 19, 22, 25, dan 28). HRTEM (Gambar S12, S17, S20, S23, S26 dan S29 , Informasi Pendukung), HAADF-STEM dan pemetaan EDS yang sesuai (Gambar S18, S21, S24, S27 dan S30 , Informasi Pendukung) menunjukkan keberhasilan persiapan RE-Pd/WO 3 . Puncak difraksi XRD sangat cocok dengan pola standar WO 3 (JCPDS NO. 33–1387, Gambar S31 , Informasi Pendukung). Setelah mendukung RE-Pd pada WO 3 , puncak difraksi yang sesuai dengan WO 3 dicadangkan, dan puncak difraksi baru muncul pada 40,1°, yang sesuai dengan faset (111) Pd (JCPDS NO. 46–1043). Pergeseran negatif puncak ini dikaitkan dengan ekspansi kisi yang timbul dari doping Ce. Puncak difraksi yang terkait dengan RE tidak teramati, yang menunjukkan bahwa RE ada sebagai atom tunggal. Spektrum Raman selanjutnya dilakukan dan ditunjukkan pada Gambar S32 (Informasi Pendukung). Puncak yang terletak di dekat 814,6 cm −1 sesuai dengan mode getaran peregangan simetris dan asimetris dari ikatan W─O─W dalam WO 3 , dan puncak yang lebih lemah di dekat 246,7 dan 325,8 cm −1 dikaitkan dengan getaran tekukan W─O. Puncak getaran W─O─W dalam Pd/WO 3 menunjukkan pergeseran biru ≈5,7 cm −1 dibandingkan dengan WO 3 . Selain itu, pergeseran biru yang lebih substansial terlihat jelas setelah doping RE, yang menunjukkan bahwa pengenalan atom RE mengubah struktur koordinasi WO 3 .
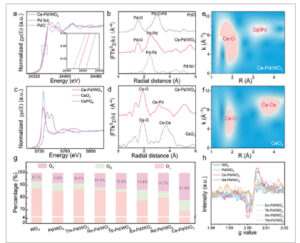
Spektroskopi serapan sinar-X (XAS) digunakan untuk menyelidiki keadaan valensi, komposisi, dan struktur koordinasi Ce-Pd/WO 3 . Seperti yang ditunjukkan pada Gambar 2a , spektrum struktur dekat tepi-K penyerapan sinar-X Pd (XANES) dari Ce-Pd/WO 3 menunjukkan pergeseran positif dibandingkan dengan foil Pd (Gambar 2a ), yang dikaitkan dengan interaksi elektron antara Pd, Ce, dan WO 3 . Spektrum struktur halus penyerapan sinar-X yang diperluas dengan Transformasi Fourier (FT-EXAFS) menunjukkan puncak yang menonjol pada 2,45 Å, yang dikaitkan dengan hamburan Pd-Pd, yang menunjukkan keberadaan Pd metalik dalam Ce-Pd/WO 3 (Gambar 2b ). Selain itu, posisi hamburan Pd-Pd menunjukkan pergeseran positif dibandingkan dengan foil Pd, yang dikaitkan dengan doping Ce. Spektrum XANES Ce L 3 -edge menunjukkan bahwa Ce-Pd/WO 3 menunjukkan puncak tunggal yang kuat, yang secara jelas berbeda dari CeO 2 dengan dua puncak maksimum yang terpisah dengan baik pada intensitas yang lebih rendah, tetapi serupa dengan yang ada di CePO 4 . Sementara itu, intensitas garis putih di Ce-Pd/WO 3 lebih rendah dari CePO 4 , yang menunjukkan keadaan oksidasi Ce mendekati 3+. Hasil EXAFS pada Gambar 2d menunjukkan bahwa puncak pada 1,92 Å sesuai dengan ikatan Ce─O, yang menunjukkan keberhasilan penggabungan Ce ke dalam WO 3 melalui pembentukan ikatan Ce─O. Puncak pada 3,16 Å sesuai dengan ikatan Ce─Pd, yang mengonfirmasi keberhasilan doping Ce dalam nanopartikel Pd. Selain itu, tidak adanya ikatan Ce─Ce pada 3,58 Å menunjukkan dispersi atomik Ce dalam Ce-Pd/WO 3 . Analisis transformasi wavelet (WT) selanjutnya mengkonfirmasi kesimpulan di atas (Gambar 2e,f ).
Gambar 2
Buka di penampil gambar
Presentasi PowerPoint
Informasi keadaan valensi dan struktur elektronik dari material yang disiapkan. a) Spektrum XANES K-edge Pd yang dinormalkan. b) Spektrum FT-EXAFS dari Pd. c) Spektrum XANES Ce L 3 -edge yang dinormalkan. d) Spektrum FT-EXAFS dari Ce. e) WT untuk sinyal EXAFS K 3 -weight Ce L 3 -edge dari Ce-Pd/WO 3 . f) WT untuk sinyal EXAFS K 3 -weight Ce L 3 -edge dari CeO 2 . g) Berbagai rasio spesies oksigen dari O 1s. h) Perbandingan spektrum EPR dalam material yang disiapkan.
Keadaan valensi dan komposisi WO 3 , Pd/WO 3 , dan RE-Pd/WO 3 diselidiki lebih lanjut dengan spektroskopi fotoelektron sinar-X (XPS). Seperti yang ditunjukkan pada Gambar S33 (Informasi Pendukung), spektrum survei XPS mengonfirmasi keberadaan unsur W, Pd, O, dan RE. Menurut spektrum XPS resolusi tinggi W 4f yang ditunjukkan pada Gambar S34 ( Informasi Pendukung), puncak dekonvolusi pada 35,7 dan 37,8 eV bersesuaian dengan W 6+ 4f 7/2 dan W 6+ 4f 5/2 dalam WO 3 , masing-masing. Energi pengikatan dalam Pd/WO 3 bergeser negatif ≈0,1 eV dibandingkan dengan WO 3 , yang menunjukkan bahwa elektron ditransfer dari Pd ke WO 3 . Lebih jauh lagi, energi pengikatan menunjukkan pergeseran yang lebih signifikan setelah doping RE, yang mengungkapkan bahwa RE lebih lanjut memodulasi struktur elektronik WO3 . Seperti yang ditunjukkan dalam spektrum Pd 3d (Gambar S35 , Informasi Pendukung), puncak kuat pada 334,9 (3d5 /2 ) dan 340,2 eV (3d3 /2 ) dikaitkan dengan Pd0 , energi pengikatan Pd0 dalam RE-Pd/WO3 semuanya bergeser positif, yang menunjukkan bahwa RE yang menggabungkan dapat meningkatkan transfer elektron dari Pd ke WO3 , yang menghasilkan peningkatan valensi untuk Pd, yang bermanfaat untuk desorpsi H. Selain itu, puncak lemah pada 336,6 (3d5 /2 ) dan 341,9 eV (3d3 /2 ) sesuai dengan Pd2 + , yang menunjukkan bahwa Pd ada terutama dalam bentuk Pd0 ; Kehadiran Pd 2+ dikaitkan dengan oksidasi permukaan yang ringan. Hasil EXAFS dan XPS menunjukkan bahwa Ce menyumbangkan elektron ke Pd, dan kemudian mentransfer dari Pd ke WO 3 . Penggabungan Ce elektronegatif rendah menginduksi interaksi elektronik antara Ce, Pd, dan WO 3 . [ 20 ] Spektrum O 1s dapat didekonvolusi menjadi tiga puncak yang terletak pada 530,6, 532,2, dan 532,8 eV, yang dikaitkan dengan oksigen kisi (O L ), kekosongan oksigen (O V ), dan oksigen yang diserap (O C ), masing-masing (Gambar S35 , Informasi Pendukung). Seperti yang ditunjukkan pada Gambar 2g , konsentrasi kekosongan oksigen meningkat setelah doping RE, yang dapat meningkatkan penyerapan O 2 dan menangkap lebih banyak elektron untuk membentuk spesies oksigen (O 2 −), dengan demikian meningkatkan desorpsi hidrogen. [ 21 ] Secara spesifik, konsentrasi kekosongan oksigen menunjukkan urutan berikut: Ce-Pd/WO 3 > Nd-Pd/WO 3 > Eu-Pd/WO 3 > Tb-Pd/WO 3 > Ho-Pd/WO 3 > Tm-Pd/WO 3 > Pd/WO 3 . Analisis EPR selanjutnya mengonfirmasi keberadaan kekosongan oksigen di semua material yang disiapkan. Dapat diamati pada Gambar 2h bahwa sinyal RE-Pd/WO 3 pada g = 2,003 lebih jelas dibandingkan dengan WO 3 dan Pd/WO 3 , dan menunjukkan tren yang sama dengan hasil XPS. Spektrum RE XPS resolusi tinggi pada Gambar S37 (Informasi Pendukung) menunjukkan bahwa RE terutama ada dalam keadaan oksidasi, yang menunjukkan bahwa RE dapat hadir sebagai atom tunggal.
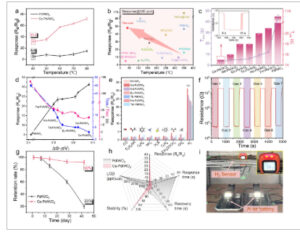
Kinerja penginderaan hidrogen dari RE-Pd/WO 3 dan Pd/WO 3 dievaluasi. Suhu pengoperasian sensor diselidiki dalam lingkungan 50 ppm H 2 . Seperti yang ditunjukkan pada Gambar 3a dan S38 (Informasi Pendukung), Pd/WO 3 dan RE-Pd/WO 3 menunjukkan peningkatan respons yang konsisten (Ra/Rg) saat suhu pengoperasian meningkat dari 40 hingga 80 °C, dan RE-Pd/WO 3 menunjukkan respons yang lebih tinggi daripada Pd/WO 3 . Peningkatan resistansi dasar dalam RE-Pd/WO 3 memberikan berbagai variasi resistansi, sehingga meningkatkan sensitivitas (Gambar S39 , Informasi Pendukung). Khususnya, sensor RE-Pd/WO 3 menunjukkan kinerja penginderaan yang luar biasa bahkan pada suhu mendekati suhu ruangan, dan Ce-Pd/WO 3 menyajikan respons tertinggi sebesar 31,3 terhadap 50 ppm H 2 , menunjukkan peningkatan 6 kali lipat daripada Pd/WO 3 dan lebih baik daripada sensor yang paling banyak dilaporkan, yang mewujudkan deteksi jejak H 2 pada suhu mendekati suhu ruangan. Suhu pengoperasian ditetapkan pada 40 °C dalam pengujian berikut untuk mencerminkan kinerja penginderaan pada suhu mendekati suhu ruangan. Hasil XRD dan TEM membuktikan stabilitas material dan integritas struktural Ce-Pd/WO₃ selama uji penginderaan hidrogen (Gambar S40 dan S41 , Informasi Pendukung). Karakteristik transisi resistif dinamis Ce-Pd/WO3 menunjukkan bahwa respons meningkat secara bertahap dari 2,8 menjadi 128,96 seiring peningkatan konsentrasi H2 dari 500 ppb menjadi 500 ppm (Gambar S42a , Informasi Pendukung), yang menunjukkan respons yang sangat baik pada konsentrasi H2 yang rendah . Konsentrasi H2 jauh lebih rendah daripada batas ledakan H2 ( 4 V/V%, 40.000 ppm), yang dapat memenuhi persyaratan aplikasi praktis. Lebih jauh lagi, respons Ce-Pd/WO 3 terhadap H 2 menunjukkan linearitas yang baik (y = 0,60586 × x +3,06553, R 2 = 0,972), dan batas deteksi (LOD) dihitung sebesar 110 ppb, yang lebih rendah daripada Pd/WO 3 (3770 ppb), yang menunjukkan bahwa sensor tersebut mampu mendeteksi H 2 pada tingkat jejak (Gambar S42c,d , Informasi Pendukung). Dibandingkan dengan berbagai sensor H 2 yang sebelumnya dilaporkan pada konsentrasi 100 ppm (Gambar 3b ; Tabel S6 , Informasi Pendukung), Ce-Pd/WOSensor 3 menunjukkan peningkatan yang signifikan pada kinerja keseluruhan. Secara khusus, waktu respons-pemulihan sensor Ce-Pd/WO3 dan Pd/WO3 masing -masing adalah 3/15 d dan 45/115 d, yang memendek 15 dan 8 kali lipat setelah penambahan Ce (Gambar 3c ). Hubungan antara respons dan waktu pemulihan respons dengan ΔФ disajikan pada Gambar 3d . Dengan penurunan ΔФ, respons meningkat, dan waktu pemulihan respons memendek. Kami selanjutnya melakukan enam percobaan replikasi (Gambar S43 , Informasi Pendukung). Hasilnya menunjukkan bahwa Ce-Pd/WO₃ memiliki pengulangan dan stabilitas yang baik.
Gambar 3
Buka di penampil gambar
Presentasi PowerPoint
Kinerja penginderaan gas dari bahan yang disiapkan. a) Respon penginderaan Pd/WO 3 dan Ce-Pd/WO 3 terhadap 50 ppm H 2 pada suhu operasi yang berbeda. b) Perbandingan sensor H 2 yang dilaporkan sebelumnya dan sensor Ce-Pd/WO 3 pada 100 ppm. c) Waktu respons-pemulihan sensor terhadap 50 ppm H 2 pada 40 °C (kurva resistansi Ce-Pd/WO 3 ). d) Perbandingan respons, waktu respons-pemulihan dalam ΔФ yang berbeda. e) Selektivitas penginderaan terhadap gas yang berbeda sebesar 50 ppm pada 40 °C. f) Interferensi-toleransi sensor Ce-Pd/WO 3 . Gas 1:50 ppm H 2 , Gas 2:50 ppm H 2 +50 ppm CH 4 , Gas 3:50 ppm H 2 +50 ppm CH 3 COCH 3 , Gas 4:50 ppm H 2 +50 ppm C 7 H 8 , Gas 5:50 ppm H 2 +50 ppm H 2 S, Gas 6:50 ppm H 2 +50 ppm +50 ppm C 2 H 5 OH +50 ppm CH 4 , dan Gas 7:50 ppm H 2 +50 ppm NH 3 +50 ppm CO +50 ppm C 6 H 6 . g) Uji stabilitas. h) Perbandingan kinerja penginderaan untuk Ce-Pd/WO 3 dan Pd/WO 3 . i) Deteksi konsentrasi H 2 dalam baterai Al-udara.
Selektivitas sensor diselidiki dalam sembilan gas pengganggu yang umum, termasuk H 2 , CH 4 , CH 3 COCH 3 , C 7 H 8 , H 2 S, NH 3 , C 6 H 6 , C 2 H 5 OH, dan CO. Seperti yang ditunjukkan pada Gambar 3e , respons terhadap H 2 adalah 10–30 kali lebih tinggi daripada molekul pengganggu lainnya, yang menunjukkan selektivitas tinggi untuk H 2 . Untuk mensimulasikan lingkungan nyata, gas pengganggu di atas dicampur dengan 50 ppm H 2 . Seperti yang ditunjukkan pada Gambar 3f , respons RE-Pd/WO 3 hampir sama dengan yang ada pada 50 ppm H 2 ketika terpapar pada atmosfer campuran, yang menunjukkan kemampuan interferensi yang unggul. Uji stabilitas pada Gambar 3g dan Gambar S44 (Informasi Pendukung) menunjukkan bahwa sensor RE-Pd/WO 3 masih mempertahankan respons tinggi setelah 42 hari, khususnya, laju retensi respons Ce-Pd/WO 3 mencapai 92%, jauh lebih tinggi daripada Pd/WO 3 (20%). Kinerja toleransi kelembapan diselidiki dalam kisaran kelembapan relatif 15%–95%, dan laju retensi respons Ce-Pd/WO 3 lebih tinggi daripada bahan olahan lainnya, yang menunjukkan stabilitas toleransi kelembapan yang lebih baik (Gambar S45 , Informasi Pendukung). Hasil di atas menunjukkan bahwa Ce-Pd/WO 3 memberikan respons tertinggi, waktu pemulihan respons terpendek, stabilitas superior, dan LoD terendah di semua bahan olahan (Gambar 3h ), dan lebih baik daripada bahan penginderaan yang paling banyak dilaporkan (Tabel S6 , Informasi Pendukung). Untuk menyelidiki kepraktisan sensor hidrogen yang dirancang, kami membuat perangkat menggunakan Ce-Pd/WO3 untuk mendeteksi konsentrasi H2 dalam baterai Al-air (Gambar 3i ; Film S1 , Informasi Pendukung). Bel berbunyi saat konsentrasi H2 mencapai 0,1 V/V%, yang jauh di bawah batas ledakan H2 , yang menunjukkan potensi aplikasi untuk deteksi H2 konsentrasi rendah pada suhu mendekati suhu ruangan.
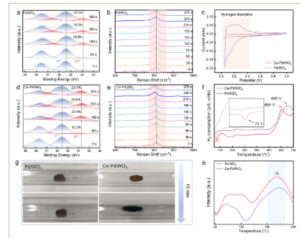
Karakterisasi lebih lanjut dilakukan untuk menunjukkan mekanisme penginderaan Hidrogen. Pertama, pengukuran XPS in situ dikumpulkan secara sistematis pada 40 °C setelah paparan H 2 . Seperti yang digambarkan pada Gambar 4d , W 5+ yang berbeda muncul hanya setelah 60 detik dalam Ce-Pd/WO 3 , dengan rasio atomik masing-masing 10,2%, 23,9%, 29,6%, dan 29,8%, yang merupakan hasil dari luapan hidrogen dari Pd ke WO 3 [ 22 ] dan mencapai kesetimbangan setelah 300 detik. Namun, W 5+ yang sesuai muncul pada 180 detik dalam Pd/WO 3 , dengan rasio atomik masing-masing 16,8%, 18,3%, dan 18,5% (Gambar 4a ), dan persentase W 5+ lebih rendah daripada yang ada di Ce-Pd/WO 3 . Hasil XPS mengungkap peran penting atom tunggal Ce dalam memfasilitasi luapan hidrogen dari Pd ke permukaan WO3 . Raman in situ dilakukan setelah paparan 50 ppm H2 pada 40 °C untuk lebih lanjut menunjukkan luapan hidrogen. Seperti yang ditunjukkan pada Gambar 4e , puncak kuat yang terletak pada 810,6 cm −1 terkait dengan vibrasi W─O─W. Menariknya, pergeseran biru puncak ini pada Ce-Pd/WO3 terjadi hanya setelah 30 detik dan meningkat seiring waktu, pergeserannya adalah ≈9,1 cm −1 setelah 270 detik paparan H2 . Namun, puncak bergeser 3,8 cm −1 pada Pd/WO3 ( Gambar 4b ), yang menunjukkan bahwa reduksi WO3 dipromosikan oleh luapan hidrogen yang difasilitasi pada Ce-Pd/ WO3 . Selama analisis voltametri siklik (CV), H yang teradsorpsi mengalami desorpsi oksidatif di daerah potensial rendah (0,05–0,4 V), yang menyebabkan munculnya puncak desorpsi hidrogen. Luapan hidrogen mengacu pada migrasi H dari situs aktif logam ke penyangga, yang dapat mengakibatkan puncak desorpsi H menurun atau menghilang. [ 23 ] Oleh karena itu, pengukuran CV dilakukan untuk menyelidiki luapan H melalui Ce-Pd/WO 3 dan Pd/WO 3 . Seperti yang ditunjukkan pada Gambar 4c , luas puncak desorpsi hidrogen di Ce-Pd/WO 3 berkurang relatif terhadap Pd/WO 3 , yang menunjukkan bahwa cakupan H pada permukaan Pd di Ce-Pd/WO 3 berkurang, dengan demikian menunjukkan terjadinya luapan H dari Pd ke WO 3 .
Gambar 4
Buka di penampil gambar
Presentasi PowerPoint
Percobaan Luapan Hidrogen. Dalam spektrum XPS dan Raman dari a,b) Ce-Pd/WO3 dan d,e) Pd-WO3 . (c) Kurva CV yang direkam dalam larutan elektrolit HClO4 0,1 m untuk Pd/ WO3 dan Ce-Pd/WO3 . f) Profil H2-TPR Pd/WO3 dan Ce -Pd/WO3 . g) Foto luapan hidrogen Pd/WO3 dan Ce-Pd/WO3 sebelum /sesudah perlakuan pada suhu 40 °C dengan aliran H2 50 mL menit −1 . h) Profil O2 – TPD Pd/WO3 dan Ce-Pd/WO3 .
Dalam percobaan reduksi terprogram suhu Hidrogen (H 2 -TPR) (Gambar 4f ), puncak negatif dekat 73 °C terkait dengan pelepasan H dari PdH x . Intensitas puncak yang lebih kuat dalam Ce-Pd/WO 3 terkait dengan lebih banyak desorpsi H, yang menunjukkan adsorpsi H yang lemah. Lebih jauh, puncak dekat 604 °C dikaitkan dengan reduksi W 6+ dalam WO 3 ; suhu reduksi dalam Ce-Pd/WO 3 menurun dibandingkan dengan Pd/WO 3 karena efek luapan H. Akhirnya, percobaan pewarnaan mengungkapkan bahwa Ce-Pd/WO 3 menunjukkan perubahan warna yang cepat daripada Pd/WO 3 , yang menunjukkan bahwa reduksi WO 3 difasilitasi oleh luapan H (Gambar 4g ). Karakterisasi di atas menunjukkan bahwa doping RE meningkatkan luapan hidrogen dalam Ce-Pd/WO 3 . Selain itu, analisis Oxygen Temperature Programmed Desorption (O 2 -TPD) dilakukan untuk mengkarakterisasi jenis spesies oksigen pada permukaan Ce-Pd/WO 3 dan Pd-WO 3 , puncak yang muncul pada 150 °C sesuai dengan desorpsi spesies O 2 − (Gambar 4h ). Khususnya, Ce-Pd/WO 3 menunjukkan intensitas puncak desorpsi O 2 − yang ditingkatkan secara signifikan dibandingkan dengan Pd/WO 3 , yang mengungkapkan kapasitas penangkapan oksigen yang unggul dan konversi selanjutnya menjadi O 2 − pada permukaan Ce-Pd/WO 3 , yang konsisten dengan hasil XPS. Karakterisasi di atas dengan kuat menunjukkan bahwa doping atom tunggal Ce memfasilitasi dua proses penting: 1) meningkatkan efisiensi luapan hidrogen melalui penurunan ΔФ, dan 2) meningkatkan konsentrasi O 2 − dengan meningkatkan konsentrasi kekosongan oksigen. Ini secara kolektif berkontribusi pada peningkatan kinerja penginderaan hidrogen dari Ce-Pd/WO 3 .
DFT dilakukan untuk menyelidiki mekanisme penginderaan gas RE-Pd/WO3 ( Gambar S46–S48 , Informasi Pendukung). Model H2 yang teradsorpsi pada Pd/WO3 dan RE-Pd/WO3 dilakukan untuk menyelidiki energi adsorpsi H2 dan energi disosiasi (Gambar S49–S52 , Informasi Pendukung). Ce-Pd/WO3 , Eu-Pd/WO3 , dan Tm-Pd/WO3 dipilih sebagai representatif. Seperti yang ditunjukkan pada Gambar 5a , energi adsorpsi (Eads) molekul H 2 dihitung sebesar -0,09 (Pd/WO 3 ), -0,28 (Eu-Pd/WO 3 ), -0,34 (Tm-Pd/WO 3 ), dan -0,36 eV (Ce-Pd/WO 3 ), yang menunjukkan adsorpsi H 2 yang kuat pada RE-Pd/WO 3 . Sementara itu, energi disosiasi untuk Pd/WO 3 , Ce-Pd/WO 3 , Eu-Pd/WO 3 , dan Tm-Pd/WO 3 masing-masing adalah -0,75, -0,11, 0,05, dan -0,09 eV. Hasil energi disosiasi menunjukkan bahwa disosiasi H 2 di semua RE-Pd/WO 3 bersifat spontan (Gambar S53–S57 dan Tabel S7 , Informasi Pendukung).
Gambar 5
Buka di penampil gambar
Presentasi PowerPoint
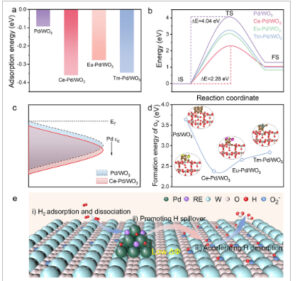
Perhitungan DFT. a) Energi adsorpsi H 2 pada Pd/WO 3 , Ce-Pd/WO 3 , Eu-Pd/WO 3 dan Tm-Pd/WO 3 . b) Energi spillover Pd/WO 3 , Ce-Pd/WO 3 , Eu-Pd/WO 3 dan Tm-Pd/WO 3 . c) Pusat pita d. d) Energi pembentukan kekosongan oksigen pada Pd/WO 3 , Ce-Pd/WO 3 , Eu-Pd/WO 3 , dan Tm-Pd/WO 3 . e) Skema mekanisme penginderaan H 2 .
Selain itu, kami juga menghitung energi struktur keadaan transisi berdasarkan jalur migrasi hidrogen dan model pada Gambar S58 dan S59 (Informasi Pendukung). Seperti yang ditunjukkan pada Gambar 5b dan Tabel S8 (Informasi Pendukung), spesies H yang teradsorpsi memerlukan penghalang energi yang lebih rendah dari luapan H dari Pd ke WO 3 dalam RE-Pd/WO 3 daripada Pd/WO 3 (4,04 eV). Secara khusus, penghalang energi luapan hidrogen berkorelasi positif dengan ΔФ; Ce-Pd/WO 3 dengan ΔФ terendah menunjukkan penghalang energi luapan hidrogen terendah (2,28 eV), yang menunjukkan mitigasi H yang paling mudah. Kepadatan keadaan (DOS) dihitung untuk menjelaskan efek doping Ce pada konfigurasi elektronik Pd. Seperti yang ditunjukkan pada Gambar 5c dan Gambar S60 (Informasi Pendukung), Ce-Pd/WO 3 menunjukkan pusat pita d yang lebih rendah (1,76 eV) daripada Pd/WO 3 (1,48 eV), yang diuntungkan oleh desorpsi H. Hasil di atas menunjukkan bahwa doping Ce dapat secara efektif mengatur ΔФ, memfasilitasi luapan dan desorpsi H. H yang dimitigasi dari Pd akan berikatan dengan spesies oksigen yang diadsorpsi pada kekosongan oksigen di WO 3 untuk membentuk H 2 O dan desorpsi, sehingga kekosongan oksigen juga penting untuk sensor hidrogen. Seperti yang ditunjukkan pada Gambar 5d dan Gambar S61 (Informasi Pendukung), energi pembentukan kekosongan oksigen dalam Pd/WO 3 , Ce-Pd/WO 3 , Eu-Pd/WO 3 , dan Tm-Pd/WO 3 masing-masing adalah 3,64, 2,37, 2,66, dan 2,84 eV, yang menunjukkan bahwa doping RE bermanfaat bagi pembentukan kekosongan. Khususnya, Ce-Pd/WO 3 menunjukkan energi pembentukan kekosongan oksigen terendah, yang menunjukkan bahwa ia memiliki konsentrasi O 2 − tertinggi , yang menghasilkan desorpsi H tercepat.
Berdasarkan hasil komputasi dan eksperimen, mekanisme penginderaan H 2 diusulkan sebagai berikut (Gambar 5e ): 1) Energi pembentukan kekosongan oksigen dalam dukungan WO 3 menurun setelah doping Ce, meningkatkan konsentrasi kekosongan oksigen. O 2 dapat diadsorpsi pada WO 3 dengan kekosongan oksigen yang melimpah, dan menjebak elektron bebas dari pita konduksi WO 3 untuk membentuk O 2 − , menghasilkan EDL yang lebih tebal di udara. Ketika Ce-Pd/WO 3 terpapar pada H 2 , molekul H 2 mudah diadsorpsi dan terdisosiasi menjadi atom hidrogen pada permukaan Pd karena energi adsorpsi hidrogen yang lebih tinggi dan energi disosiasi negatif dari H 2 . 2) Doping Ce mengurangi ΔФ antara Pd dan WO 3 , yang mengarah pada penurunan penghalang energi luapan H, sehingga memfasilitasi mitigasi H dari Pd ke WO 3 . 3) Atom-atom H yang dimitigasi mudah bereaksi dengan spesies O 2 − permukaan yang ditingkatkan untuk membentuk H 2 O, yang disertai dengan pelepasan elektron kembali ke WO 3 , sehingga mengakibatkan pengurangan lebar dan resistansi EDL.
3 Kesimpulan
Singkatnya, sekelompok material RE-Pd/WO₃ disiapkan untuk meningkatkan kinerja penginderaan H 2 dalam konsentrasi rendah pada suhu mendekati suhu kamar. Perhitungan DFT mengungkapkan bahwa modifikasi atom tunggal RE pada Pd dapat menyesuaikan perbedaan fungsi kerja antara Pd dan WO₃, dan penghalang energi migrasi hidrogen berkurang dari 4,04 eV (Pd/WO 3 ) menjadi 2,28 eV (Ce-Pd/WO 3 ) seiring berkurangnya perbedaan fungsi kerja, yang mempercepat luapan hidrogen dari Pd ke WO₃. Eksperimen Raman in situ, XPS in situ, dan luapan hidrogen mengonfirmasi luapan hidrogen yang difasilitasi pada Ce-Pd/WO 3 dibandingkan dengan Pd/WO 3 . Sementara itu, RE atomik juga memicu penurunan energi pembentukan kekosongan oksigen, yang menghasilkan peningkatan spesies oksigen pada WO 3 , yang bermanfaat bagi desorpsi hidrogen. Hasilnya, RE-Pd/WO3 menunjukkan kinerja penginderaan H2 yang jauh lebih baik daripada Pd/WO3 , dan Ce-Pd/WO3 dengan perbedaan fungsi kerja terendah (0,44 eV) dan energi pembentukan kekosongan oksigen (2,37 eV) memberikan kinerja penginderaan tertinggi. Ce-Pd/WO₃ menunjukkan respons 31,3 terhadap 50 ppm H₂, yang 6 kali lebih tinggi daripada Pd/WO₃. Selain itu, perangkat yang dibuat dengan Ce-Pd/WO3 juga menghadirkan respons cepat untuk kebocoran hidrogen dalam baterai Al-air, yang menunjukkan aplikasi potensial untuk deteksi H2 konsentrasi rendah pada suhu mendekati suhu kamar. Pekerjaan ini menyoroti modulasi yang tepat dari perbedaan fungsi kerja pada percepatan luapan hidrogen dan dapat memberikan panduan teoritis dan eksperimental untuk mengembangkan sensor H2 efisiensi tinggi . Di masa mendatang, universalitas strategi ini harus diselidiki lebih lanjut untuk pengembangan bahan penginderaan oksida logam.

