
Abstrak
Perovskit ganda halida baru-baru ini telah menarik minat yang signifikan dalam aplikasi konversi energi surya karena sifatnya yang tidak beracun dan penyerapan surya yang tinggi. Namun, distorsi struktural yang tidak diantisipasi dalam bahan-bahan ini dapat membahayakan kinerjanya, menekan distorsi struktural sangat penting dan tetap menjadi tantangan. Di sini, dilaporkan bahwa penggunaan feniletilamin yang memicu transisi fase ketidakteraturan-keteraturan dapat secara signifikan meningkatkan tingkat keteraturan oktahedra dalam perovskit ganda Cs 2 AgBiBr 6 , yang dapat menekan eksiton dan cacat yang terperangkap sendiri dan memungkinkan pemisahan muatan cepat, yang mengarah ke sifat foto-fisika/kimia yang luar biasa dengan peningkatan fotoaktivitas lebih dari enam kali lipat dalam aktivasi ikatan C−H fotokatalitik dibandingkan dengan struktur yang kurang teratur. Pekerjaan ini memberikan strategi yang efektif untuk memecahkan masalah yang menantang dari fenomena ketidakteraturan perovskit ganda halida untuk meningkatkan konversi energi surya-ke-kimia.
1 Pendahuluan
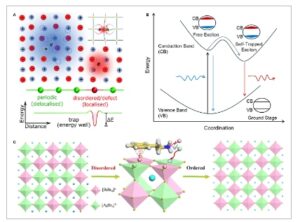
Perovskit halida (HP) telah menarik perhatian luar biasa dalam aplikasi fotoelektronik dalam dekade terakhir karena sifat optoelektroniknya yang fantastis. [ 1 – 3 ] Hingga saat ini, efisiensi konversi daya sel surya HP telah meroket hingga 26%, [ 4 ] setara dengan teknologi silikon. Selain sel surya, HP juga memegang janji besar dalam dioda pemancar cahaya, [ 5 , 6 ] fotodetektor, [ 7 , 8 ] fotokatalisis, [ 9 , 10 ] dan perangkat penyimpanan/memori. [ 11 , 12 ] Meskipun perovskit berbasis timbal, seperti halida timbal metilamonium, telah menunjukkan potensi besar untuk aplikasi optoelektronik, stabilitas dan toksisitas yang buruk dari sebagian besar HP berbasis Pb membatasi aplikasi lebih lanjut mereka. [ 13 , 14 ] Baru-baru ini, perovskit ganda halida anorganik A 2 B I B III X 6 telah muncul sebagai alternatif bebas timbal yang menjanjikan. Di antara mereka, Cs 2 AgBiBr 6 (CABB), suatu senyawa dengan celah pita yang sesuai, waktu hidup pembawa mikrodetik, dan stabilitas lingkungan yang unggul, telah memicu banyak perhatian. [ 13 ] Meskipun demikian, karena proses sintesis larutan menggunakan prekursor kation (yaitu, CsBr, AgBr, dan BiBr 3 ), pembentukan fase yang sebagian tidak teratur dengan susunan acak [AgBr 6 ] 5− dan [BiBr 6 ] 3− oktahedra tidak dapat dihindari dan secara energetik menguntungkan, [ 15 ] yang mengarah pada peningkatan tolakan elektrostatik antara oktahedra yang berdekatan ( Gambar 1A ), [ 16 ] mendistorsi struktur kristal yang berasal dari distorsi seperti Jahn–Teller. [ 15 , 17 ] Akibatnya, interaksi kuat antara elektron dan fonon menjebak pembawa muatan yang dihasilkan foto dalam keadaan terdistorsi, membentuk eksiton yang terperangkap sendiri (STF) yang menghambat transportasi muatan (Gambar 1B ). [ 15 , 16 , 18 ] Selain itu, gangguan dalam hunian kation menghasilkan Ag Bicacat antisit dalam celah pita, menciptakan pusat rekombinasi untuk pembawa muatan (Gambar 1C ). [ 15 , 18 , 19 ]
Gambar 1
Buka di penampil gambar
Presentasi PowerPoint
Efek transisi fase pada dinamika muatan. A) Skema yang mengilustrasikan muatan yang terperangkap dalam kisi yang terdistorsi dan lokalisasi muatan yang dihasilkan dari ketidakteraturan non-periodik dan cacat kisi. B) Diagram yang menggambarkan eksiton bebas yang terperangkap sendiri melalui potensi deformasi. C) Skema yang mewakili kerapatan keadaan (DOS) dalam semikonduktor yang tidak teratur. D) Skema transisi fase ketidakteraturan-orde yang dimediasi ligan PEA dari material CABB. Gambar 1A : Direproduksi dengan izin dari Ref. [ 16 ] dan Ref. [ 18 ] Hak Cipta 2023, Wiley-VCH; Hak Cipta 2020, The Royal Society of Chemistry. Gambar 1B : Direproduksi dengan izin dari Ref. [ 16 ] Hak Cipta 2023, Wiley-VCH.
Rekayasa struktur telah secara signifikan memajukan pemisahan pembawa muatan fotogenerasi yang efisien dalam semikonduktor. [ 17 , 20 , 21 ] Secara teoritis, teori fungsi kerapatan (DFT) digunakan untuk menyelidiki transisi fase ketidakteraturan-keteraturan dalam subkisi campuran dari parameter pemesanan. [ 22 – 24 ] Misalnya, Zhang et al. melakukan DFT untuk mendapatkan wawasan tentang bagaimana konfigurasi kation Ag + /Bi 3+ memengaruhi struktur elektronik Cs 2 AgBiX 6 (X = Br, Cl). [ 24 ] Demikian pula, Yang et al. menunjukkan bahwa ketidakteraturan Ag–Bi dalam CABB memengaruhi struktur pita melalui hibridisasi pita. [ 23 ] Secara eksperimental, menggabungkan ligan/polimer sebagai pengikat selektif lokasi dalam oksida perovskit ganda telah terbukti meningkatkan pemesanan kation. Khususnya, awan elektron π-fenil berinteraksi dengan orbital σ* dari Bi-X melalui efek yang diinduksi elektron-dorong, [ 25 ] memfasilitasi ikatan dengan ion Bi 3+ . Selain itu, pembentukan makrosiklus kiral kompleks enantioselektif yang dikaitkan dengan pengenalan enantiomerik meningkatkan ikatan amina halogenasi aromatik dengan Ag + . [ 26 ] Terinspirasi oleh temuan ini, pengenalan ligan yang cocok dapat meningkatkan tatanan kisi CABB. Yang menggembirakan, feniletilamonium (PEA) telah dilaporkan membantu regulasi kristal dalam CABB dengan meningkatkan tatanan Ag + /Bi 3+ , [ 15 , 17 , 27 , 28 ] yang mengarah pada peningkatan struktur kisi dan sifat optoelektronik. Efek ini dapat dikaitkan dengan kombinasi koordinasi selektif, interaksi elektrostatik, dan relaksasi regangan kisi. Secara khusus, PEA lebih suka berkoordinasi dengan Ag + dan Bi 3+ , menstabilkan posisi mereka dan mengurangi ketidakteraturan kation. Lebih jauh, PEA dapat memengaruhi lingkungan elektrostatik lokal, yang mendorong struktur teratur yang stabil secara termodinamika. Meskipun ada kemajuan ini, efek transisi fase dalam CABB pada aplikasinya dalam konversi energi surya ke kimia masih jarang dieksplorasi.
Dalam penelitian ini, kami berfokus pada perovskit ganda halida yang umum, CABB. Pengaturan in situ dari transisi fase order-disorder dalam CABB menggunakan ligan phenylethylamine bromide (PEABr) digunakan untuk meningkatkan pemesanan kation Ag + /Bi 3+ , yang menghasilkan perbedaan dramatis dalam sifat fotolistrik dan katalitik. Secara khusus, struktur yang teratur menunjukkan pemisahan muatan yang lebih baik dan energi penghalang yang berkurang dalam reaksi fotoredoks permukaan dibandingkan dengan yang kurang teratur. Dengan memanfaatkan transisi fase, CABB yang dimodifikasi secara drastis meningkatkan kinerja fotokatalitik saat menguji aktivasi ikatan benzilik C(sp 3 )−H dalam toluena di bawah cahaya matahari yang disimulasikan.
2 Hasil dan Pembahasan
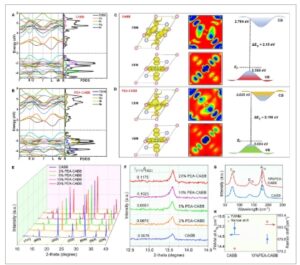
Gambar 1C mengilustrasikan efek PEA pada susunan oktahedra [AgBr 6 ] 5− dan [BiBr 6 ] 3− dari CABB (PEA-CABB). Investigasi teoritis menggunakan kalkulasi DFT pertama kali dilakukan untuk memeriksa perubahan dalam struktur elektronik CABB yang dipengaruhi oleh pengurutan kation, [ 29 , 30 ] termasuk struktur pita, densitas keadaan (DOS), dan distribusi muatan ( Gambar 2 ; Gambar S1 , Informasi Pendukung). Pemeriksaan karakteristik sel (a) dan volume struktur CABB dan PEA-CABB mengungkapkan bahwa setelah modifikasi PEA dari CABB, nilai “ a ” meningkat sedikit dari 11,23 menjadi 11,28 Å, dan volume meningkat dari 1417,50 menjadi 1433,65 Å 3 . Melihat stabilitas relatif dari kedua sistem ini menunjukkan bahwa struktur PEA-CABB lebih stabil daripada CABB, dengan energi total -119,0963 eV untuk struktur PEA-CABB dan -118,93057 eV untuk CABB. Spektrum kepadatan keadaan total (TDOS) dan kepadatan keadaan terproyeksi yang diselesaikan atom (PDOS) memberikan analisis struktur elektronik yang lebih rinci. Gambar 2A, B mengilustrasikan efek PEA dalam PEA-CABB, di mana orbital Ag 4d berhibridisasi dengan orbital Br 4p untuk berkontribusi bersama pada VBM sementara orbital Bi 6p menempati CBM. Pengenalan PEA mengarah pada celah pita yang sedikit ditingkatkan, berubah dari 2,15 menjadi 2,19 eV, di mana celah pita untuk kedua struktur tidak langsung (Gambar 2C, D ). Ini mendukung eksperimen mengenai evolusi celah pita yang lebih lebar setelah memperkenalkan PEA (vide infra). Peta kerapatan muatan terkait CBM dan VBM dari sel primitif CABB dan PEA-CABB ditunjukkan pada Gambar 2C,D . Berbeda dengan kerapatan muatan CABB, PEA-CABB menunjukkan kerapatan muatan terkait CBM dan VBM yang lebih besar dan lebih dispersif, yang disebabkan oleh susunan Ag + dan Bi 3+ yang lebih teratur . [ 17 ]
Gambar 2
Buka di penampil gambar
Presentasi PowerPoint
Investigasi struktural yang menggabungkan kalkulasi teoritis dan karakterisasi eksperimental. A,B) Struktur pita dan PDOS dan C,D) distribusi muatan CBM dan VBM dari sistem CABB dan PEA-CABB, masing-masing. E) Pola XRD CABB dan serangkaian sampel PEA-CABB dengan konsentrasi PEA + prekursor yang berbeda. F) Puncaknya sesuai dengan bidang (111) relatif terhadap intensitas bidang (022). G) Spektrum Raman dan H) FWHM dari mode A 1g dan pergeseran Raman dari sampel CABB dan 10%PEA-CABB.
Berikutnya, kami bergerak untuk mensintesis material dan memeriksa sifat fotoelektroniknya secara eksperimental. Proses sintesis CABB dijelaskan dalam bagian Eksperimen. Prosedur serupa diadopsi untuk mensintesis CABB yang teratur, kecuali memanfaatkan kemampuan pengompleksan ligan PEA + dengan ion Ag + dan Bi 3+ untuk meningkatkan pengurutan hunian kation. Secara khusus, awan elektron π dari gugus fenil dalam PEA + cenderung berikatan dengan orbital σ* dari Bi 3+ karena mekanisme yang diinduksi oleh elektron dorong. [ 25 ] Sementara itu, gugus amonium dari PEA + membentuk ikatan dengan Ag + melalui gaya antarmolekul nonkovalen. Keterkaitan yang disukai ini difasilitasi oleh kesamaan jarak antara gugus fenil dan amonium dalam PEA + (6,4 Å), [ 17 ] dan jarak antara Ag + dan Bi 3+ dalam CABB (6,5 Å). Akibatnya, oktahedra [AgBr 6 ] 5− dan [BiBr 6 ] 3− terstruktur secara periodik, yang pada akhirnya membentuk CABB yang teratur.
Penilaian kuantitatif dari tatanan kation dalam perovskit ganda dapat dicapai dengan mengevaluasi pola difraksi sinar-X (XRD) dari sampel. [ 15 , 17 ] Secara umum, CABB termasuk dalam grup ruang Fm3̅m dan struktur kristal menyimpang dari hukum kepunahan konvensional untuk bidang (111) dan (022). Untuk Ag + dan Bi 3+ yang sepenuhnya tidak teratur , bidang (111) akan punah. [ 17 ] Oleh karena itu, mempelajari intensitas bidang (111) dan (022) (yaitu, I 111 /I 022 ) adalah pendekatan yang ampuh untuk menganalisis tingkat tatanan dalam CABB. Semakin tinggi rasionya, semakin baik tatanan oktahedra [AgBr 6 ] 5− dan [BiBr 6 ] 3− dan lebih sedikit cacat antisit Ag Bi . Ini telah diakreditasi dalam struktur perovskit ganda tersebut. [ 31 , 32 ]
Gambar 2E menunjukkan pola XRD sampel CABB dan PEA-CABB dengan berbagai konsentrasi prekursor PEABr. Semua sampel menunjukkan puncak difraksi yang sama, di mana tidak ada bahan berbasis PEA seperti PEA4AgBiBr8 yang terbentuk, yang menunjukkan bahwa pengenalan PEA tidak memengaruhi struktur intrinsik CABB. Selain itu , semua sampel PEA-CABB menunjukkan pergeseran puncak yang dapat diabaikan dibandingkan dengan CABB murni, yang menunjukkan efek regangan minimal. Perhatikan bahwa PEA + dapat tetap melekat pada senyawa dengan ikatan koordinat setelah pembentukan CABB yang teratur, dan ligan dapat didesorpsi pada suhu tinggi seperti 280 °C. [ 15 ] Namun, perubahan terlihat saat menganalisis intensitas dan lebar puncak secara kuantitatif secara terperinci. Intensitas bidang (111) relatif terhadap bidang (022) meningkat seiring dengan peningkatan konsentrasi PEA (Gambar 2F ), yang menunjukkan peningkatan dalam urutan hunian Ag + dan Bi3 + . [ 17 ] Sementara itu, lebar penuh pada setengah maksimum (FWHM) bidang (111) menurun saat konsentrasi PEA + meningkat, yang menunjukkan peningkatan penataan kation dan berkurangnya densitas cacat Ag Bi dalam sampel PEA-CABB. [ 17 ] Hal ini didukung oleh pengukuran Raman (Gambar 2G ). Berdasarkan penataan struktural maksimum dan aktivitas fotokatalitik yang diamati dalam rentang yang diuji (vide infra), sampel PEA-CABB 10% dipilih untuk karakterisasi eksperimen. Spektrum Raman dari CABB asli menunjukkan puncak yang kuat pada 180 cm −1 , yang dikaitkan dengan mode fonon optik longitudinal (LO) A 1g , bersamaan dengan getaran peregangan simetris Br di sekitar atom Bi. [ 33 ] Dua puncak lain pada bilangan gelombang yang lebih rendah juga terdeteksi. Puncak pada 139 cm −1 ditetapkan ke mode E 1g , yang sesuai dengan getaran peregangan asimetris Br di sekitar atom Bi. Sementara itu, mode T 2g pada 74 cm −1 terkait dengan gerakan menggunting Cs di sekitar atom Br. Di sini, kami fokus pada mode A 1g karena bertanggung jawab atas kopling elektron-fonon dan distorsi kisi kristal. [ 15 ] Dibandingkan dengan CABB tak beraturan murni, penurunan yang nyata dalam FWHM mode LO dalam sampel 10%PEA-CABB representatif dan sedikit pergeseran puncak ke arah energi yang lebih tinggi diamati (Gambar 2H ). Pengamatan ini juga telah dilaporkan dalam sistem lain,[ 34 ] memperkuat kesimpulan adanya peningkatan keteraturan dalam hunian kation.
Spektroskopi fotoelektron sinar-X (XPS) dilakukan untuk menyelidiki struktur kimia dan keadaan valensi material. Gambar S2B (Informasi Pendukung) menunjukkan dua puncak Cs 3d karakteristik pada 738,1 dan 724,1 eV, yang masing-masing sesuai dengan Cs 3d 3/2 dan Cs 3d 5/2 . [ 35 ] Tidak ada perubahan yang diamati untuk sampel PEA-CABB. Pergeseran serupa juga dicatat dalam Ag 3d, Bi 4f, dan Br 3d (Gambar S2C–E , Informasi Pendukung). Lebih jauh lagi, tidak adanya puncak N 1s dalam PEA-CABB (Gambar S2F , Informasi Pendukung) menunjukkan bahwa PEA tidak tergabung dalam kisi atau membentuk senyawa berbasis PEA. Spektroskopi fotoelektron ultraviolet (UPS) mengungkapkan sedikit perubahan pada batas elektron sekunder dan tepi pita valensi dari kedua sistem ini (Gambar S3 , Informasi Pendukung). Spektroskopi inframerah transformasi Fourier (FTIR) menunjukkan interaksi antara PEA dan Ag + /Bi 3+ (Gambar S4 , Informasi Pendukung). Mikroskop elektron pemindaian (SEM) mengungkapkan morfologi permukaan yang serupa untuk bahan CABB dan PEA-CABB (Gambar S5 , Informasi Pendukung), dan spektroskopi sinar-X dispersif energi (EDS) mengonfirmasi keberadaan elemen yang sama. Gambar mikroskop elektron transmisi (TEM) menunjukkan bahwa CABB dan PEA-CABB memiliki struktur partikel yang sebanding (Gambar S6 , Informasi Pendukung), dengan jarak kisi dalam bidang (200) sebesar 0,32 nm, yang selaras dengan parameter kisi CABB yang diketahui. [ 36 ] Pemetaan EDS menunjukkan elemen Cs, Ag, Bi, dan Br di seluruh sampel PEA-CABB (Gambar S7 , Informasi Pendukung).
Sifat penyerapan optik dari CABB dan PEA-CABB murni diperiksa menggunakan spektroskopi refleksi difusi UV–vis. Spektrum penyerapan CABB menunjukkan tepi pita penyerapan pada 595 nm ( Gambar 3A ). Setelah memperkenalkan PEA, pergeseran biru sedikit diamati (foto optik ditunjukkan pada Gambar S8 , Informasi Pendukung), yang mungkin disebabkan oleh peningkatan pemesanan kation dalam struktur perovskit ganda. [ 17 ] Pengamatan ini sejalan dengan temuan sebelumnya, [ 23 , 37 ] di mana sistem yang teratur menunjukkan ambang batas penyerapan cahaya yang lebih tinggi daripada yang tidak teratur.
Gambar 3
Buka di penampil gambar
Presentasi PowerPoint
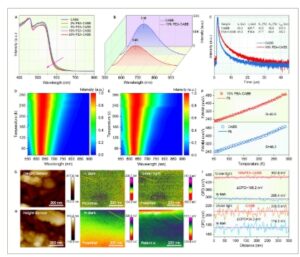
Sifat optik dan elektronik. A) Spektrum DRS UV–vis dari CABB dan serangkaian sampel PEA-CABB. B) Spektrum PL keadaan stabil, C) peluruhan PL yang diselesaikan waktu, D,E) PL yang bergantung pada suhu pseudocolor, F) FWHM dari puncak PL sebagai fungsi suhu, G,H) Gambar potensial AFM dan KPFM dalam iradiasi gelap dan terang, dan I) Kurva SPV yang sesuai dari bahan CABB dan 10%PEA-CABB, masing-masing.
Sifat fotofisika bahan CABB dan PEA-CABB diselidiki lebih lanjut melalui spektroskopi fotoluminesensi (PL). Spektrum PL kondisi tunak CABB menunjukkan puncak emisi pada sekitar 646 nm (Gambar 3B ). Tidak ada perubahan emisi PL terkait cacat yang diamati dalam sampel PEA-CABB, yang menunjukkan bahwa kerapatan cacat tetap relatif tidak berubah. Intensitas PL yang lebih rendah diamati dalam PEA-CABB dibandingkan dengan CABB, yang menunjukkan rekombinasi radiatif yang ditekan dan dengan demikian pengurangan jalur rekombinasi yang tidak diinginkan untuk pembawa muatan yang dihasilkan foto. [ 38 , 39 ] Hal ini didukung oleh data PL beresolusi waktu (Gambar 3C ), di mana peluruhan PL sampel dianalisis menggunakan model bi-eksponensial, dengan konstanta peluruhan yang diekstraksi τ 1 dan τ 2 masing-masing sesuai dengan rekombinasi eksiton terikat dan eksiton bebas. [ 10 , 40 ] Sampel PEA-CABB menunjukkan waktu hidup yang lebih panjang daripada CABB murni, dengan kontribusi τ 1 menurun dari 43,2% (64 ns) menjadi 37,7% (85 ns), sementara kontribusi τ 2 meningkat dari 56,8% menjadi 62,3% dengan τ 2 memanjang dari 635 menjadi 976 ns. Rekombinasi eksiton yang ditekan dan waktu hidup pembawa yang ditingkatkan dikaitkan dengan pemisahan elektron-lubang yang cepat, memberikan bukti yang jelas tentang pemisahan muatan yang lebih efektif untuk PEA-CABB. Penelitian sebelumnya telah menunjukkan bahwa susunan Ag + dan Bi 3+ yang tidak teratur dalam senyawa perovskit ganda menyebabkan interaksi elektron-fonon yang kuat. [ 15 ]
Untuk lebih memahami efek pengurutan Ag + /Bi 3+ dalam kasus kami, pengukuran PL yang bergantung pada suhu dilakukan (Gambar 3D,E ; Gambar S9 , Informasi Pendukung). Kopling elektron-fonon dievaluasi secara kuantitatif menggunakan faktor Huang-Rhys (S), yang diperoleh dari FWHM puncak PL menurut persamaan: [ 17 ]
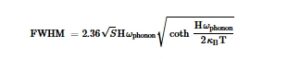
di mana ω fonon adalah frekuensi fonon, T adalah suhu, dan k B adalah konstanta Boltzmann. Seperti yang ditunjukkan pada Gambar 3F , nilai S dari CABB murni dan PEA-CABB ditentukan masing-masing sebesar 48,2 dan 43,6. Biasanya, nilai S yang lebih tinggi menunjukkan kecenderungan yang lebih besar untuk pembentukan STE. [ 17 ] Analisis di atas mengungkapkan peningkatan sifat fotolistrik dalam sistem PEA-CABB.
Mikroskopi gaya probe Kelvin (KPFM) selanjutnya dilakukan untuk mengamati potensial permukaan CABB dan PEA-CABB sebelum dan setelah paparan cahaya. [ 41 ] Gambar AFM (Gambar 3G,H ) menunjukkan CABB dengan ukuran nanopartikel yang sebanding yaitu beberapa ratus nanometer. Profil garis yang sesuai dari perbedaan potensial kontak (CPD) gambar dalam gelap dan di bawah iluminasi cahaya PEA-CABB adalah sekitar 176,2 mV (Gambar 3I ), secara signifikan lebih tinggi daripada CABB (34,2 mV), memverifikasi bahwa lebih banyak akumulasi muatan fotogenerasi pada permukaan PEA-CABB sebagai peningkatan pemisahan muatan. Untuk lebih memahami mekanisme di balik peningkatan pemisahan muatan, spektroskopi impedansi elektrokimia (EIS) digunakan untuk menyelidiki perubahan sifat perpindahan muatan sampel (Gambar S10 , Informasi Pendukung). Berdasarkan plot Nyquist, resistansi perpindahan muatan ( R ct ) dari PEA-CABB (11,3 kΩ) secara signifikan lebih rendah dibandingkan dengan CABB (21,1 MΩ), yang menunjukkan bahwa penambahan PEA meningkatkan konduktivitas listrik pada CABB, [ 10 ] sehingga meningkatkan perpindahan muatan.
Sifat fotoelektronik sampel kemudian dinilai menggunakan oksidasi toluena fotokatalitik sebagai reaksi model (Gambar S11 , Informasi Pendukung, lihat bagian Eksperimental), dengan kinerja fotokatalitik dirangkum dalam Gambar 4A . Tidak ada produk reaksi yang terdeteksi tanpa adanya fotokatalis dan penyinaran cahaya. Setelah 4 jam penyinaran cahaya, CABB murni menghasilkan benzaldehida (BAD) pada laju produksi 905,2 µmol g −1 h −1 , dengan jumlah kecil benzil alkohol (BA) sebagai produk sampingan utama (125,3 µmol g −1 h −1 ), menghasilkan selektivitas BAD sebesar 87,8%. Sebaliknya, bahan PEA-CABB menunjukkan peningkatan yang signifikan dalam fotoaktivitas. Laju produksi BAD tertinggi sebesar 5801,6 µmol g −1 h −1 dicapai dengan senyawa 10%PEA-CABB dengan selektivitas 92,8%, yang merupakan peningkatan 6,4 kali lipat dibandingkan CBB asli. Pengukuran GC-MS mengonfirmasi produk BAD dan BA yang dihasilkan (Gambar S12 , Informasi Pendukung), dan tidak ada produk sampingan potensial lainnya (misalnya, asam benzoat) yang terdeteksi. Perhatikan bahwa PEA di atas 20% menyebabkan penurunan kinerja fotokatalitik, mungkin karena pemisahan muatan yang lebih rendah dan berkurangnya situs aktif. Yang penting, sampel 10%PEA-CABB yang dioptimalkan mengungguli fotokatalis yang paling baru dilaporkan (Gambar 4B ; Tabel S1 , Informasi Pendukung).
Gambar 4
Buka di penampil gambar
Presentasi PowerPoint
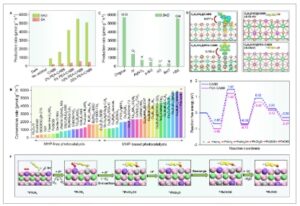
Evolusi aktivitas fotokatalitik dan studi mekanisme reaksi. A) Kinerja fotokatalitik oksidasi toluena pada katalis CABB dan x %PEA-CABB. B) Eksperimen kontrol dengan pemulung yang berbeda. C) Perbandingan aktivitas fotokatalitik oksidasi toluena pada material 10%PEA-CABB dan fotokatalis lain yang baru-baru ini dilaporkan. D) Plot perbedaan kerapatan muatan dari penyerapan toluena pada katalis dan analisis muatan Bader (panel kiri), dan energi penyerapan antara katalis dan produk BAD (panel kanan). E) Energi bebas Gibbs untuk CABB dan PEA-CABB. F) Ilustrasi skematis dari proses fotooksidasi toluena pada katalis PEA-CABB.
Untuk menjelaskan mekanisme reaksi ini, percobaan pelabelan isotop dilakukan. Menggunakan toluena terdeuterasi (d 8 -toluena) sebagai reaktan mengungkapkan efek isotop kinetik (KIE) dengan rasio k H / k D sebesar 3,3 (Tabel S2 , Informasi Pendukung), yang menunjukkan bahwa pembelahan ikatan C(sp 3 )-H dalam toluena adalah langkah penentu laju. [ 42 , 43 ] Selain itu, spektrum GC-MS dari produk terdeuterasi dirangkum dalam Gambar S13 (Informasi Pendukung). Percobaan kontrol dengan pemulung dilakukan lebih lanjut untuk lebih memahami mekanisme reaksi (Gambar 4C ). Amonium oksalat (AO), perak nitrat (AgNO 3 ), 1,4-benzoquinone (p-BQ), t-butanol (t-BA), dan butilat hidroksitoluena (BHT) digunakan sebagai pemulung untuk lubang (h + ), elektron (e − ), superoksida ( • O 2 − ), hidroksil ( • OH − ), dan radikal berpusat karbon ( • R), masing-masing, untuk menyelidiki efeknya pada fotooksidasi toluena. [ 44 – 46 ] Pemulung lubang fotogenerasi dengan AO menyebabkan penurunan yang signifikan dalam efisiensi konversi toluena. Kehadiran pemulung elektron AgNO 3 mengurangi laju reaksi tetapi tidak sepenuhnya menghentikannya. Penambahan p-BQ juga mengakibatkan penurunan laju konversi. Di sisi lain, penggantian O 2 dengan Ar hampir menghentikan reaksi sama sekali. Perhatikan bahwa AgNO3 memiliki efek penghambatan yang lebih signifikan pada laju reaksi daripada gas Ar. Efek serupa diamati dengan pengenalan pemulung radikal BHT, sedangkan penambahan t-BA memiliki dampak minimal pada laju reaksi. Percobaan ini menyoroti pentingnya radikal bebas dan menunjukkan bahwa elektron dan lubang yang dihasilkan foto memainkan peran penting dalam aktivasi toluena.
Resonansi paramagnetik elektron (EPR) digunakan untuk mengidentifikasi spesies oksigen reaktif yang dihasilkan, menggunakan 5,5-dimetil-1-pirolina N-oksida (DMPO) sebagai agen penangkap (Gambar S14 , Informasi Pendukung). Dalam gelap, sinyal DMPO- • O 2 − yang sangat lemah terekam, tanpa konversi toluena yang terjadi dalam kondisi ini. Setelah terpapar radiasi cahaya, sinyal EPR spesies • O 2 − terdeteksi, dengan kekuatan sinyal meningkat seiring waktu iluminasi diperpanjang, yang menunjukkan bahwa elektron fotogenerasi dalam katalis PEA-CABB mereduksi O 2 menjadi • O 2 − . Selain itu, tanda tangan kuat yang sesuai dengan radikal nitroksida terdeteksi setelah radiasi yang lama, yang dihasilkan dari pembelahan ikatan N─C dan pembukaan cincin aduk DMPO- • O 2 − . Berdasarkan pengamatan ini, mekanisme yang masuk akal untuk fotooksidasi selektif toluena menjadi BAD melalui fotokatalis PEA-CABB diusulkan: [ 45 , 46 ] di bawah penyinaran cahaya, PEA-CABB menyerap cahaya matahari dengan energi foton tertentu, menghasilkan pasangan elektron-lubang. Elektron ditransfer ke permukaan fotokatalis, mereduksi oksigen molekuler yang diserap menjadi spesies • O 2 − ; sementara itu, lubang mengoksidasi substrat toluena menjadi karbokation. Karbokation radikal toluena kemudian bereaksi dengan spesies • O 2 − untuk menghasilkan produk BAD.
Stabilitas bahan 10%PEA-CABB juga dinilai. Gambar S15A (Informasi Pendukung) menunjukkan fotoaktivitas yang tidak terganggu setelah lima siklus berturut-turut dibandingkan dengan kinerja awalnya, yang menunjukkan stabilitas bahan ini yang baik. Pola XRD (Gambar S15B , Informasi Pendukung) semakin menegaskan struktur kristal katalis yang terpelihara dengan baik, yang menunjukkan stabilitasnya yang tinggi.
Untuk mengembangkan pemahaman mendalam tentang peningkatan fotoaktivitas dalam sistem PEA-CABB pada tingkat molekuler, perhitungan DFT dilakukan untuk merinci reaksi fotoredoks permukaan. Perbedaan kerapatan muatan dan analisis muatan Bader pertama kali dihitung untuk memeriksa populasi muatan dan transfer antara katalis dan reaktan yang diadsorpsi (Gambar 4D ; Gambar S16 dan S17 , Informasi Pendukung). Hasilnya menunjukkan bahwa transfer muatan dari PEA-CABB ke molekul toluena lebih besar daripada sampel CABB, yang menunjukkan aktivasi reaktan yang lebih baik dan dengan demikian memfasilitasi konversi toluena menjadi produk BAD utama. [ 47 , 48 ] Lebih jauh lagi, PEA-CABB menunjukkan kemampuan adsorpsi yang lebih kuat dari perantara reaktan (Gambar S18 , Informasi Pendukung) dan desorpsi BAD yang lebih lemah dibandingkan dengan CABB (Gambar 4D , panel kanan), yang bermanfaat untuk meningkatkan fotoaktivitas. [ 49 ] Energi bebas Gibbs pada langkah-langkah elementer diselidiki lebih lanjut, dengan diagram energi ditunjukkan pada Gambar 4E . Studi perbedaan kerapatan muatan elektron menunjukkan interaksi permukaan yang tidak dapat diamati antara molekul toluena yang teradsorpsi dan permukaan katalitik (Gambar S16 dan S17 , Informasi Pendukung). PEA-CABB menunjukkan interaksi yang lebih kuat antara atom H dan Bi karena jaraknya yang lebih pendek (2,71Å) dan distribusi muatan yang terlokalisasi. Hal ini memiringkan molekul toluena ke arah atom Bi, memfasilitasi disosiasi ikatan C─H (Gambar 4F ). Energi bebas Gibbs untuk penyerapan dan aktivasi molekul toluena pada CABB dan PEA-CABB dihitung. Energi adsorpsi negatif menunjukkan bahwa adsorpsi molekul toluena pada katalis ini lebih hemat energi. Meskipun disosiasi ikatan C─H merupakan proses yang sedikit menanjak, PEA-CABB memiliki penghalang energi aktivasi yang lebih rendah (1,22 eV) daripada CABB (1,47 eV), yang menunjukkan proses konversi tolina yang jauh lebih cepat pada PEA-CABB. Analisis muatan Bader digunakan untuk menjelaskan variasi energi aktivasi ini. Muatan yang ditransfer dari PEA-CABB ke zat antara *PhCH2 lebih besar daripada muatan CABB (Gambar 4D ), yang menunjukkan bahwa reaktan molekul tolina lebih teraktivasi dan *PhCH3 diubah menjadi *PhCH2 dengan lebih mudah. Lebih jauh lagi, semua langkah reaksi selanjutnya secara energetik menguntungkan (Gambar 4E ) kecuali untuk produksi *PhCH2O . Khususnya, sistem PEA-CABB menunjukkan penghalang energi yang lebih rendah untuk pembentukan zat antara, termasuk langkah pembatas laju *PhCH2 generasi (Gambar S19 , Informasi Pendukung), dibandingkan dengan CABB asli, sehingga mengurangi hambatan energi untuk keseluruhan proses oksidasi. Hasilnya, adsorpsi dan aktivasi molekul toluena lebih disukai secara termodinamika, meningkatkan oksidasi fotokatalitik toluena. [ 49 ] Berdasarkan hasil, jalur konversi fotooksidasi toluena melalui fotokatalis PEA-CABB, dengan struktur adsorpsi zat antara, diilustrasikan pada Gambar 4F dan Gambar S20 (Informasi Pendukung).
3 Kesimpulan
Singkatnya, mengatur susunan [AgBr6 ] 5− dan [BiBr6 ] 3− oktahedra meningkatkan tingkat pemesanan oktahedra dalam CABB. Peningkatan ini menghilangkan eksiton yang terperangkap sendiri dan cacat antisit AgBi , sehingga mengurangi lokalisasi kuat pasangan elektron-lubang dan rekombinasi muatan. Secara eksperimental, transisi fase ini dicapai melalui modifikasi ligan PEA. Material yang ditata ulang menunjukkan efisiensi pemisahan muatan yang lebih unggul dibandingkan dengan CABB asli. Hasilnya, peningkatan sifat fotolistrik intrinsik dari material yang tertata fase menyebabkan peningkatan signifikan dalam kinerja oksidasi toluena fotokatalitik, lebih dari enam kali lipat lebih tinggi daripada sampel yang kurang tertata. Secara keseluruhan, koordinasi selektif ion fenil dan amonium yang difungsionalisasi dalam PEA⁺ memfasilitasi pembentukan susunan tertata bergantian dari ion Ag + dan Bi3 + . Peningkatan penataan oktahedra [AgX 6 ] 5 ⁻ dan [BiX 6 ] 3 ⁻ ini, yang telah divalidasi secara teoritis dan eksperimental, memainkan peran penting dalam modulasi celah pita dan pengurangan kerapatan cacat dibandingkan dengan AgBiBr 6 Cs 2 murni . Lebih jauh lagi, tingkat penataan Ag + /Bi 3+ yang tinggi secara signifikan menekan pembentukan eksiton yang terperangkap sendiri, yang mengarah pada peningkatan mobilitas pembawa, faktor kunci dalam meningkatkan kinerja optoelektronik. Studi ini menyoroti hubungan antara struktur kristal dan fotoaktivitas dalam perovskit ganda halida, yang menawarkan wawasan berharga untuk memahami sifat fotolistrik bahan-bahan ini, yang juga dapat menginformasikan penelitian yang melibatkan kecerdasan buatan. [ 50 ]
4 Bagian Eksperimen
Bahan
Cesium bromida (CsBr, 99,9%), bismuth(III) bromida (BiBr 3 , ≥98%), perak bromida (AgBr, ≥99,9%), feniletilamina bromida (PEABr, ≥98%), dimetil sulfoksida (DMSO, anhidrat, ≥99,9%), isopropanol (IPA, ≥99,5%, reagen ACS), dan toluena (anhidrat, 99,8%) dibeli dari Sigma–Aldrich. Semua bahan kimia digunakan tanpa pemurnian lebih lanjut.
Persiapan Sampel
Sintesis Cs2AgBiBr6 : Cs2AgBiBr6 disintesis menggunakan proses larutan suhu kamar melalui pendekatan presipitasi antipelarut. Secara khusus, 319,2 mg CsBr, 336,5 mg BiBr3 , dan 140,8 mg AgBr pertama-tama dilarutkan dalam 5 mL larutan DMSO dalam rasio molar stoikiometris (yaitu, CsBr:AgBr:BiBr3 = 2 : 1 : 1 ) pada konsentrasi 0,15 m untuk membentuk prekursor Cs2AgBiBr6 . Kemudian, larutan prekursor yang telah disiapkan ditambahkan ke 40 mL IPA untuk mendapatkan suspensi Cs2AgBiBr6 melalui metode presipitasi antipelarut. Suspensi tersebut selanjutnya disentrifugasi untuk mengumpulkan Cs2AgBiBr6 , yang kemudian dikeringkan semalaman dalam oven vakum pada suhu 60 °C. Hasilnya, dapat diperoleh 796,5 mg bubuk Cs2AgBiBr6 dengan hasil hampir 100% .
Sintesis PEA- Cs2AgBiBr6 : Sintesis PEA- Cs2AgBiBr6 mengikuti prosedur yang sama seperti Cs2AgBiBr6 , dengan pengecualian bahwa sebagian CsBr digantikan oleh PEABr (dalam rasio 2, 5, 10, dan 20 mol % ) . Secara spesifik, PEABr (6,1, 15,2, 30,5, dan 31,0 mg untuk 2, 5, 10, dan 20% PEA-Cs 2 AgBiBr 6 sampel, masing-masing) bersama dengan CsBr (312,8, 303,2, 287,3, dan 255,4 mg untuk 2, 5, 10, dan 20% PEA-Cs 2 AgBiBr 6 sampel, masing-masing), BiBr 3 (329,8, 319,7, 302,9, dan 269,2 mg untuk 2, 5, 10, dan 20% PEA-Cs 2 AgBiBr 6 sampel, masing-masing) dan AgBr (138,0, 133,9, 126,7, dan 112,6 mg untuk 2, 5, 10, dan 20% sampel PEA- Cs2AgBiBr6 , masing – masing ) bubuk kemudian dilarutkan dalam 5 mL DMSO untuk membentuk larutan prekursor.
Karakterisasi
Data XRD diperoleh menggunakan difraktometer sinar-X (radiasi Cu Kα1, λ = 1,5406 Å) dengan sampel 100 mg yang dipasang pada tempat sampel serbuk. Mikrograf elektron pemindaian (SEM) direkam menggunakan mikroskop elektron pemindaian FEI-Q FEG250, di mana serbuk 10 mg diletakkan pada potongan sampel dengan pita karbon konduktif. Gambar mikroskop elektron transmisi (TEM) diambil pada JEOL ARM200F, menggunakan sampel serbuk 5 mg yang didispersikan dalam larutan IPA 5 dan larutan 10 µL yang diteteskan ke kisi tembaga TEM. Pengukuran fotoluminesensi (PL) keadaan tunak dilakukan menggunakan spektrometer Edinburgh FLS980, memindai sampel serbuk (100 mg dalam kuvet kuarsa) dari 500 hingga 900 nm dalam langkah 2 nm dengan waktu integrasi 1 detik, di bawah eksitasi pada 405 nm. Data PL yang diselesaikan waktu direkam menggunakan mikroskop confocal FLIM, dengan sampel bubuk 50 mg pada substrat kaca kuarsa. Eksitasi disediakan oleh dioda laser 405 nm berdenyut (LDH-DC-485), dengan filter bandpass (Chroma ET485/20x). Laju pengulangan laser ditetapkan ke 1 MHz menggunakan driver PDL 828 Sepia2 (PicoQuant). Spektrum serapan optik diperoleh menggunakan spektrofotometer reflektansi difusi (DRS) UV–vis (Shimadzu UV-2600i) dengan rentang deteksi 400–800 nm, dengan sampel bubuk 50 mg dan barium sulfat (BaSO 4 ) sebagai referensi. Spektroskopi fotoelektron sinar-X (XPS) dilakukan menggunakan instrumen Thermo Scientific Nexsa dengan sumber sinar-X Al Kα monokromatik pada 1486,68 eV, menggunakan sampel bubuk 20 mg, dan puncak dikalibrasi dengan spektrum C 1s pada 284,8 eV. Pengukuran mikroskopi gaya atom (AFM) dilakukan menggunakan mikroskopi gaya atom (Seiko, sistem Bioscope) dengan mode semikontak, di mana bubuk 25 mg dilapisi pada substrat kaca kuarsa, Data perbedaan potensial kontak (CPD) diperoleh menggunakan mikroskopi gaya probe Kelvin (KPFM) dalam mode AM-SKM dual-pass. Spektroskopi penyerapan transien femtodetik dilakukan pada spektroskopi pompa-probe optik dengan penguat laser Ti-safir mode terkunci, dan sampel disiapkan dengan pelapisan putar larutan prekursor 50 µL 0,1 m ke substrat kuarsa. Percobaan pembersihan radikal dilakukan dengan menggunakan amonium oksalat (AO), perak nitrat (AgNO 3 ), 1,4-benzoquinone (p-BQ), t-butanol (t-BA), dan butilat hidroksitoluena (BHT) sebagai pembersih lubang (h + ), elektron (e − ), superoksida ( • O 2 − ), hidroksil ( • OH − ), dan radikal berpusat karbon ( • R), masing-masing, di mana 0,5 m m pembersih ditambahkan ke sistem reaksi dengan waktu reaksi 4 jam.
Evaluasi Aktivitas Fotokatalitik
Percobaan fotooksidasi toluena dilakukan dalam reaktor kuarsa 25 mL di bawah simulasi pencahayaan cahaya matahari. Secara khusus, 10 mg fotokatalis ditambahkan ke 2,5 mL toluena dengan oksigen molekuler jenuh, diikuti oleh penyinaran selama 4 jam sambil diaduk. Setelah itu, campuran disentrifugasi, dan cairan dianalisis dengan GC (Shimadzu 2010).
Perhitungan Teori Fungsi Kepadatan
Semua perhitungan dilakukan menggunakan metode gelombang tertambah proyektor (PAW) dan teori fungsional kerapatan terpolarisasi spin (DFT) sebagaimana diterapkan dalam paket simulasi ab-initio Vienna (VASP). Jumlah atom yang sama digunakan dalam sistem CABB dan PEA-CABB. Interaksi pertukaran-korelasi antara elektron dijelaskan menggunakan variasi aproksimasi gradien umum (GGA) Perdew–Burke–Ernzerhof (PBE). Untuk konvergensi tensor tegangan optimal selama relaksasi parameter, dipilih batas gelombang bidang sebesar 550 eV. Zona Brillouin diambil sampelnya dengan jaring titik-G berpusat bergantung ukuran, yaitu, 3 × 3 × 3 untuk sel satuan Cs8Ag4Bi8Br24 dan Cs8Ag4Bi8Br24 terdoping PEA dan untuk sel super Cs8Ag4Bi8Br24 (001) dan struktur PEA- Cs8Ag4Bi8Br24 ( 001 ) , digunakan 1 × 3 × 1. Untuk mencegah interaksi antara gambar periodik , area vakum sekitar 15 Å dibuat di atas lapisan permukaan. Parameter kisi dan posisi atomik dilonggarkan sepenuhnya hingga variasi energi total berada dalam 10 −4 eV dan gaya akhir pada setiap atom kurang dari 0,01 eV Å −1 . Koreksi van der Waals diperiksa untuk fungsional vdW menggunakan metode Grimme bersama dengan peredaman Becke–Jonson. [ 51 ] Analisis muatan Bader dilakukan dengan menganalisis kerapatan muatan elektronik menggunakan skema Bader Henkelman. [ 52 ] Sifat-sifat listrik, khususnya kerapatan keadaan (DOS), diprediksi menggunakan fungsional HSE12. Secara umum, fungsional hibrida (seperti HSE06) memprediksi celah pita dan struktur listrik yang lebih realistis daripada fungsional murni (seperti PBE). Perhitungan dilakukan menggunakan fungsional HSE12 dengan kontribusi pertukaran tepat 12%. Karena HSE12 membutuhkan banyak daya pemrosesan, hanya titik Gamma yang diambil sampelnya di zona Brillouin untuk perhitungan HSE12.
Persamaan yang digunakan untuk menentukan energi adsorpsi molekul organik (OM) pada permukaan Cs8Ag4Bi8Br24 ( 001 ) dan PEA- Cs8Ag4Bi8Br24 ( 001 ) adalah sebagai berikut :
![]()
di mana E OM merupakan singkatan dari energi total molekul organik terisolasi dalam fase gas dan E Surf+OM dan E Surf merupakan energi total dengan dan tanpa adsorpsi molekul organik pada permukaan, masing-masing.
Selain itu, perbedaan antara perbedaan kerapatan muatan 2D dan 3D dari struktur-struktur ini (Δ ρ ) dihitung. Perbedaan kerapatan muatan dihitung menggunakan persamaan berikut:
![]()
Di sini, ρ [Surf + OM] adalah total kerapatan muatan molekul organik yang teradsorpsi pada permukaan kompleks yang sesuai, ρ [Surf] dan ρ [OM] adalah kerapatan muatan lempeng permukaan Cs 8 Ag 4 Bi 8 Br 24 (001) dan PEA-Cs 8 Ag 4 Bi 8 Br 24 (001), dan masing-masing molekul organik

