
Abstrak
Mengembangkan katalis bebas logam golongan platina (PGM) yang tahan lama sangat penting untuk memungkinkan produksi hidrogen yang hemat biaya melalui elektroliser air membran pertukaran anion (AEMWE). Di sini, studi ini menyajikan katalis NiMo yang dienkapsulasi dalam cangkang karbon yang rusak. Sementara katalis NiMo konvensional terdegradasi dengan cepat dalam kondisi intermiten dengan perubahan tegangan, katalis NiMo yang dienkapsulasi karbon menunjukkan ketahanan yang luar biasa terhadap degradasi dengan aktivitas reaksi evolusi hidrogen (HER) yang baik, secara efektif mengatasi tantangan yang terkait dengan integrasi energi terbarukan. Cangkang karbon mencegah penonaktifan yang disebabkan oleh oksidasi dengan menghambat transformasi struktural Ni metalik menjadi hidroksida yang menyertai ekspansi volumetrik dalam kondisi tegangan rangkaian terbuka. Dengan menggunakan AEMWE yang terintegrasi dengan elektroda referensi, kontribusi kelebihan potensial dipisahkan dan menunjukkan bahwa stabilitas katalis HER menentukan operasi AEMWE yang tahan lama dalam skenario intermiten. Studi ini menetapkan strategi untuk pengembangan katalis bebas PGM yang tahan lama untuk produksi hidrogen yang berkelanjutan dan berskala.
1 Pendahuluan
Krisis iklim yang sedang terjadi mengharuskan adanya peralihan global menuju sistem energi netral karbon, dengan sumber-sumber energi terbarukan seperti tenaga surya dan angin yang memimpin transisi ini. [ 1 ] Meskipun menjanjikan, sifat sumber-sumber energi ini yang tidak menentu memerlukan penyimpanan energi yang andal dan solusi pembawa energi, seperti hidrogen, untuk mengatasi ketidaksesuaian antara pasokan dan permintaan. [ 2 ] Sebagai solusinya, elektrolisis air yang didukung oleh kelebihan listrik terbarukan telah muncul sebagai teknologi utama untuk produksi hidrogen hijau. [ 3 ]
Di antara berbagai teknologi elektrolisis, elektroliser air membran penukar anion (AEMWE) secara unik menggabungkan keunggulan elektroliser air alkali (AWE) dan elektroliser air membran penukar proton (PEMWE). [ 4 ] AEMWE menggunakan logam transisi yang melimpah di bumi dan berbiaya rendah seperti Ni sambil mencapai efisiensi energi yang tinggi dan kemurnian hidrogen melalui desain rakitan elektroda membran (MEA). [ 5 ] Meskipun memiliki keunggulan ini, tidak adanya komponen MEA yang terstandarisasi, termasuk membran, ionomer, dan katalis, membatasi skalabilitas AEMWE. [ 6 , 7 ]
Pengembangan katalis terus menjadi hambatan yang signifikan, khususnya untuk reaksi evolusi hidrogen (HER) di katode. [ 8 , 9 ] Sementara katalis Ni(Fe) oksida/hidroksida unggul dalam reaksi evolusi oksigen (OER) pada anoda, pengembangan alternatif bebas logam golongan platina (PGM) untuk Pt/C untuk HER tetap menantang. [ 10 – 12 ] Kemajuan terkini telah menyoroti potensi paduan berbasis Ni, khususnya NiMo, sebagai katalis HER bebas PGM berkinerja tinggi dalam AEMWE. [ 12 – 21 ] Namun, sebagian besar penelitian berfokus pada operasi berkelanjutan pada kerapatan arus tinggi, mengabaikan degradasi dalam kondisi intermiten realistis yang merupakan ciri khas sumber energi terbarukan. [ 12 – 19 ]
Penelitian ini membahas degradasi katoda berbasis NiMo dalam operasi intermiten. Kami mengidentifikasi bahwa transformasi Ni yang disebabkan oleh oksidasi ireversibel menyebabkan degradasi dalam tegangan rangkaian terbuka (OCV), dan mengusulkan strategi enkapsulasi karbon yang mudah untuk meningkatkan stabilitas katalis. Dengan mengintegrasikan elektroda referensi dalam AEMWE, kami memisahkan kontribusi tegangan lebih dan menunjukkan efektivitas katalis NiMo yang dienkapsulasi karbon dalam mengurangi degradasi. Temuan ini berkontribusi pada pengembangan katalis bebas PGM yang tahan lama dan hemat biaya untuk produksi hidrogen yang berkelanjutan.
2 Hasil dan Pembahasan
2.1 Paduan NiMo Berbungkus Karbon
Paduan Ni3Mo disintesis menggunakan metode kopresipitasi dengan sedikit modifikasi pada pekerjaan kami sebelumnya (dirinci dalam bagian eksperimen). [ 20 ] Untuk membungkus paduan Ni3Mo dengan karbon, gas CO dimasukkan langsung setelah proses reduksi dalam tungku tabung pada suhu 330 °C. Disproporsionasi CO, yang dikenal sebagai reaksi Boudouard, menghasilkan karbon unsur, yang diendapkan sebagai cangkang tipis di sekitar partikel Ni3Mo . Waktu perlakuan CO bervariasi dari 10 hingga 300 menit, seperti yang dilambangkan dalam nama katalis (misalnya, Ni3Mo @ C60 menunjukkan 60 menit perlakuan CO).
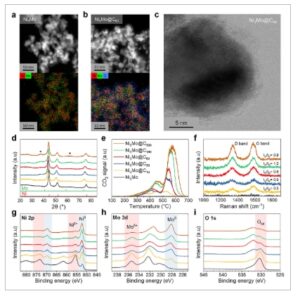
Mikroskopi elektron transmisi (TEM) mengonfirmasi bahwa ukuran rata-rata partikel hanya sedikit meningkat dari 16,6 nm pada Ni 3 Mo polos menjadi 21,2 nm pada Ni 3 Mo@C 300 bahkan setelah perlakuan CO reduktif selama 300 menit, yang mengindikasikan bahwa cangkang karbon mencegah agregasi partikel (Gambar S1 , Informasi Pendukung). Pembentukan cangkang karbon menjadi jelas saat waktu perlakuan CO meningkat; sementara Ni 3 Mo@C 10 menunjukkan cangkang karbon yang sangat tipis, Ni 3 Mo@C 60 menyajikan cangkang yang jauh lebih tebal ( Gambar 1 a–c ; Gambar S2 , Informasi Pendukung). Analisis spektrometri massa plasma yang digabungkan secara induktif (ICP-MS) dan spektroskopi sinar-X dispersif energi (EDS) menunjukkan rasio molar Ni:Mo yang konsisten sebesar ≈3:1 di seluruh katalis, yang sesuai dengan komposisi prekursor awal (Tabel S1 , Informasi Pendukung). Pola difraksi sinar-X (XRD) mengungkapkan puncak-puncak Ni metalik dengan sedikit pergeseran ke bawah, yang disebabkan oleh paduan dengan Mo (Gambar 1d ).
Gambar 1
Buka di penampil gambar
Kekuatan Gambar
Karakterisasi struktur katalis Ni 3 Mo dan Ni 3 Mo@C x . Gambar pemetaan TEM dan EDS dari (a) Ni 3 Mo dan (b) Ni 3 Mo@C 60 . (c) Gambar TEM resolusi tinggi terkoreksi Cs dari Ni 3 Mo@C 60 . (d) Pola XRD. Tanda bintang dalam XRD mewakili spesies Mo karbida/oksikarbida. e) Analisis TPO, dan (f) Spektrum Raman dari cangkang karbon. Spektrum XPS pada (g) Ni 2p, h) Mo 3d, dan (i) O 1s. Wilayah merah menunjukkan spesies teroksidasi dan wilayah biru menunjukkan spesies logam.
Analisis oksidasi terprogram suhu (TPO) mengukur kandungan karbon dari katalis Ni 3 Mo@C x , yang meningkat dari 0,026 hingga 0,173 mg karbon /mg katalis dengan waktu perlakuan CO yang diperpanjang (Gambar 1e ). Semua katalis menunjukkan peningkatan sinyal CO 2 dalam dua wilayah suhu: 300 – 500 °C (sinyal karbon rusak) dan 500–700 °C (sinyal karbon grafit), dengan kedua intensitas sinyal berkorelasi dengan durasi perlakuan CO (Gambar S3 dan Tabel S2 , Informasi Pendukung). Perilaku ini menunjukkan bahwa paparan CO yang berkepanjangan menghasilkan cangkang karbon multi-lapis yang lebih tebal sambil mempertahankan karakteristik cacat bawaannya. Spektroskopi Raman selanjutnya mendukung pengamatan ini, menunjukkan rasio I D /I G yang konsisten di semua sampel, yang menandakan bahwa sifat cacat cangkang karbon tetap tidak berubah meskipun ketebalannya meningkat (Gambar 1f ; Tabel S3 , Informasi Pendukung).
Enkapsulasi karbon secara efektif melindungi inti paduan logam dari oksidasi yang disebabkan udara. Analisis spektroskopi fotoelektron sinar-X (XPS) dari spektrum Ni 2p dan Mo 3d mengungkapkan bahwa Ni 3 Mo menampilkan kontribusi substansial dari spesies teroksidasi (Ni 2+ / Ni 3+ dan Mo 6+ ), sedangkan katalis Ni 3 Mo@C x dengan cangkang karbon sebagian besar mempertahankan keadaan logamnya, dengan kontribusi oksidasi minimal (Gambar 1g,h ). Lebih jauh lagi, katalis Ni 3 Mo@C x dengan waktu perlakuan CO yang lebih lama menunjukkan sinyal yang lebih kecil yang biasanya dikaitkan dengan oksigen kisi oksida logam dalam spektrum XPS O 1s (Gambar 1i ). Yang penting, tingkat oksidasi pada permukaan inti paduan berkorelasi terbalik dengan waktu perlakuan CO. Bukti lebih lanjut tentang sifat logam disediakan oleh spektrum struktur tepi dekat penyerapan sinar-X (XANES) di tepi K Ni dan Mo. Ni 3 Mo menunjukkan intensitas garis putih tertinggi untuk Ni K-edge, yang menunjukkan spesies teroksidasi, sedangkan waktu perlakuan CO yang lebih lama mengurangi fitur ini dan menggeser posisi Mo K-edge, yang menandakan peningkatan sifat metalik (Gambar S4 , Informasi Pendukung). [ 22 , 23 ]
Perlakuan CO yang berkepanjangan menyebabkan dealloying minor. Enkapsulasi karbon yang berlebihan mengakibatkan pengeluaran Mo dari inti paduan, sebagaimana dibuktikan oleh pergeseran ke posisi puncak XRD yang lebih tinggi untuk Ni(111), yang mengakibatkan dealloying parsial (Gambar S5 , Informasi Pendukung). Analisis menggunakan hukum Vegard memperkirakan bahwa komposisi inti paduan berubah dari Ni3Mo 1,25 dalam Ni3Mo @ C10 menjadi Ni3Mo 0,80 dalam Ni3Mo @ C60 menjadi Ni3Mo 0,42 dalam Ni3Mo @ C300 , sedangkan Ni3Mo polos menunjukkan dealloying yang lebih besar dengan komposisi Ni3Mo 0,28 karena pembentukan oksida asli (Tabel S4 , Informasi Pendukung) . Katalis Ni3Mo @Cx dengan perlakuan CO yang lebih lama menunjukkan jarak radial Ni-Ni yang berkurang, dibandingkan dengan Ni3Mo @ C10 , dalam spektrum struktur halus serapan sinar-X (EXAFS) tepi-K Ni yang terbobot k3 , yang selanjutnya menunjukkan dealloying parsial ( Gambar S6 , Informasi Pendukung). Evolusi puncak kecil dalam XRD pada 37,4° dan 61,6° untuk katalis Ni3Mo @ Cx juga menunjukkan pembentukan karbida Mo (α-MoCx ) atau oksikarbida Mo (MoOC) dalam cangkang karbon (Gambar 1d ). [ 24 , 25 ]
Secara keseluruhan, perlakuan CO yang terkontrol menghasilkan katalis Ni 3 Mo@C x dengan jumlah cangkang karbon yang bervariasi. Tingkat kerusakan lapisan karbon tetap tidak berubah berapa pun jumlahnya. Cangkang karbon yang membungkus mempertahankan sifat logam inti paduan dengan mencegah oksidasi yang disebabkan oleh udara.
2.2 Aktivitas HER Elektrokimia dan Stabilitas Ni3Mo @ Cx dalam Media Alkali
Aktivitas HER elektrokimia katalis Ni3Mo @ Cx dievaluasi dalam elektrolit KOH 1 M yang dibersihkan dengan Ar menggunakan pengaturan tiga elektroda. Larutan KOH 1 m dimurnikan menurut prosedur yang disarankan sebelumnya untuk menghilangkan spesies Fe jejak yang dapat memengaruhi sinyal elektrokimia dari katalis. [ 26 ] Hasil voltametri sapuan linier (LSV) awal menunjukkan bahwa Ni3Mo menunjukkan aktivitas HER yang lebih tinggi dibandingkan dengan katalis Ni3Mo @ Cx ( Gambar 2a ) . Overpotensial awal meningkat seiring dengan bertambahnya waktu perlakuan CO, kemungkinan disebabkan oleh lintasan difusi reaktan yang memanjang melalui cangkang karbon berpori. Situs aktif sebenarnya dari paduan NiMo masih belum jelas, dan penelitian terbaru menunjukkan pelarutan dinamis dan penyerapan kembali spesies Mo pada substrat Ni sebagai asal dari aktivitas HER yang tinggi. [ 27 – 30 ] Meskipun dealloying parsial dapat mengubah komposisi permukaan, jumlah total spesies Mo yang berpartisipasi dalam reaksi adalah sama untuk semua katalis. Percobaan keracunan CO selanjutnya menegaskan bahwa inti logam paduan, bukan lapisan karbon, yang menyediakan situs aktif (Gambar S7 , Informasi Pendukung). Ketika inti logam paduan dilindi dengan mengaduk katalis dalam asam nitrat pada suhu 60 °C selama 12 jam, cangkang karbon hanya tertinggal bersama spesies Mo yang tersisa (Gambar S8 , Informasi Pendukung). Katalis yang terukir tidak menunjukkan aktivitas HER dalam 1 m KOH, yang juga menunjukkan bahwa inti logam paduan berfungsi sebagai situs aktif HER primer (Gambar S9 , Informasi Pendukung).
Gambar 2
Buka di penampil gambar
Kekuatan Gambar
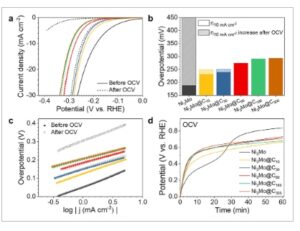
Aktivitas HER dan stabilitas katalis Ni 3 Mo dan Ni 3 Mo@C x sebelum dan sesudah pemberian tegangan rangkaian terbuka (OCV) selama 1 jam dalam 1 M KOH. Perubahan (a) voltametri sapuan linier (LSV), b) overpotensial pada −10 mA cm −2 , dan (c) kemiringan Tafel katalis Ni 3 Mo dan Ni 3 Mo@C x diperoleh sebelum dan sesudah penuaan. d) Perubahan potensial setelah pemberian OCV selama 1 jam.
Stabilitas di bawah operasi terputus-putus, yang melibatkan paparan tegangan rangkaian terbuka (OCV), sangat penting untuk katalis elektrolisis air dalam aplikasi praktis. Untuk mengevaluasi ini, katalis Ni3Mo @ Cx diuji setelah penuaan selama 1 jam dalam 1 M KOH di bawah rangkaian terbuka. Ni3Mo menunjukkan degradasi yang signifikan, kehilangan hampir semua aktivitas HER, sementara katalis Ni3Mo @ Cx menunjukkan retensi yang sangat baik, dengan cangkang karbon yang lebih tebal (misalnya, Ni3Mo @ C60 , Ni3Mo @ C180 , dan Ni3Mo @ C300 ) mempertahankan aktivitas awalnya sepenuhnya (Gambar 2a ; Gambar S10 , Informasi Pendukung). Overpotensial pada -10 mA cm -2 untuk Ni3Mo meningkat dari 189,1 menjadi 450,0 mV setelah paparan rangkaian terbuka (Gambar 2b ). Sebaliknya, katalis dengan cangkang karbon yang lebih tebal (Ni3Mo @ C60 , Ni3Mo @ C180 , dan Ni3Mo @C300) menunjukkan perubahan overpotensial yang dapat diabaikan, yang menunjukkan stabilitas yang unggul. Kemiringan Tafel juga sebagian besar tidak terpengaruh untuk katalis Ni3Mo@Cx (Gambar 2c; Tabel S5, Informasi Pendukung). Sebagai katalis dengan aktivitas dan daya tahan tinggi, Ni3Mo @ C60 , yang tidak menunjukkan degradasi setelah penuaan bersama dengan overpotensial terendah , dipilih dan digunakan untuk karakterisasi lebih lanjut dan pengujian sel tunggal.
Peran cangkang karbon dalam mengurangi degradasi diselidiki lebih lanjut dengan memantau perubahan potensial selama periode penuaan (Gambar 2d ). Ni3Mo menunjukkan infleksi yang jelas dalam potensial, sedangkan katalis Ni3Mo @ Cx tidak menunjukkan perilaku tersebut. Potensi pada titik infleksi Ni3Mo sangat selaras dengan puncak yang diamati selama pemindaian anodik pertama voltametri siklik ( Gambar 3a ,b ; Gambar S11 , Informasi Pendukung). Puncak ini, ditunjukkan dengan simbol berlian pada Gambar 3b dan Gambar S11b (Informasi Pendukung), telah dikaitkan dengan pembentukan α-Ni(OH) 2 dalam penelitian sebelumnya. [ 31 ]
Gambar 3
Buka di penampil gambar
Kekuatan Gambar
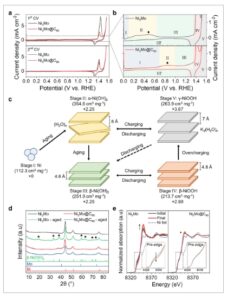
Transformasi fase Ni 3 Mo dan penekanan oksidasi pada katalis Ni 3 Mo@C x dalam 1 M KOH. a) Voltametri siklik (CV) katalis Ni 3 Mo dan Ni 3 Mo@C x yang mengilustrasikan transisi fase dari Ni metalik menjadi hidroksida. b) Tampilan CV pertama yang diperbesar. Daerah berwarna dengan angka Romawi menunjukkan jendela potensial yang berbeda dari transisi fase. Simbol berlian menunjukkan potensi puncak untuk transformasi menjadi α-Ni(OH) 2 . c) Representasi skematis dari transisi fase reversibel dan ireversibel Ni, yang diperluas dari siklus Bode asli, dengan volume spesifik dan keadaan oksidasi rata-rata yang ditunjukkan. Warna diagram sesuai dengan daerah transisi fase. d) Pola XRD katalis Ni 3 Mo dan Ni 3 Mo@C 60 setelah penuaan selama 24 jam dalam 1 m KOH. Simbol sekop menunjukkan evolusi puncak yang sesuai dengan β-Ni(OH) 2 . e) Spektra Operando Ni K-edge XANES dari katalis Ni 3 Mo dan Ni 3 Mo@C 60 yang diperoleh dengan OCV.
Secara khusus, voltamogram siklik (CV) dapat dibagi menjadi enam wilayah, yang masing-masing mewakili rentang potensial untuk tahap spesifik transformasi fase Ni (Gambar 3b ). Pada tahap I, segera setelah HER, katalis mempertahankan sifat metalik dan aktivitas HER. Pada tahap II, transformasi dari fase metalik ke fase α-Ni(OH) 2 terjadi secara spontan dalam 1 m KOH di bawah OCV dengan kinetika lambat dalam orde menit hingga jam. Proses ini dapat dipercepat dengan potensial yang diberikan. Pada tahap III, fase α-Ni(OH) 2 berubah secara ireversibel menjadi fase β-Ni(OH) 2 bahkan tanpa menerapkan potensial eksternal. [ 32 – 34 ] Sapuan anodik tambahan ke potensial yang lebih tinggi menyebabkan oksidasi dan deprotonasi lebih lanjut, membentuk β-NiOOH pada tahap IV, yang kemudian berubah menjadi γ-NiOOH yang aktif dalam reaksi evolusi oksigen (OER) pada tahap V. [ 35 ]
Selama pemindaian katoda pertama kembali dari 1,55 V RHE ke 0 V RHE , transformasi reversibel dari γ/β-NiOOH ke β-Ni(OH) 2 diamati pada ≈1,35 V RHE (tahap III’). Di sini (tahap III’), tidak ada indikasi kembali ke fase α-Ni(OH) 2 atau fase Ni metalik melalui reduksi yang diamati. Tidak adanya puncak anoda dalam pemindaian anoda berikutnya mengonfirmasi ketidakterbalikan transformasi fase β-Ni(OH) 2 menjadi α-Ni(OH) 2 atau Ni metalik (Gambar S12 , Informasi Pendukung). Transformasi spontan Ni 3 Mo dari fase metalik menjadi fase α-Ni(OH) 2 , yang dengan mudah dan ireversibel berubah menjadi fase β-Ni(OH) 2 setelah penuaan, secara dominan menyebabkan hilangnya aktivitas HER dalam elektrolit KOH. Proses-proses ini dirangkum dalam sebuah skema, yang merupakan versi diperluas dari siklus Bode asli (Gambar 3c ). [ 32 ]
Transformasi fase Ni3Mo dalam 1M KOH setelah perubahan potensial juga dipantau menggunakan spektroskopi Raman in situ (Gambar S13 , Informasi Pendukung). Puncak yang muncul dari Ni(OH) 2 diamati setelah merendam elektroda kerja dalam 1m KOH dan menerapkan 0V RHE , yang menunjukkan pembentukan cepat Ni hidroksida di permukaan. Ketika potensial dinaikkan ke 1,45V RHE , dua puncak muncul pada 474 cm −1 dan 556 cm −1 , yang masing-masing sesuai dengan mode getar tekuk Eg dan mode getar regangan A1g dari NiIII -O dari NiOOH, yang menunjukkan transformasi fase menjadi Ni oksihidroksida. [ 36 ] Puncak lebar ≈1050 cm −1 mengonfirmasi pembentukan γ-NiOOH yang aktif-OER. [ 37 ] Ketika potensial diturunkan dari 1,45V RHE , puncak Ni(OH) 2 muncul lagi. Menariknya, dua puncak NiOOH bertahan hingga 1,1 V RHE , yang mungkin menunjukkan bahwa transformasi reduktif kembali ke Ni hidroksida mungkin tidak langsung terjadi. Kedua puncak NiOOH akhirnya menghilang ketika potensial diturunkan melampaui 1,05 V RHE , dan kembali sepenuhnya ke Ni(OH) 2. Secara keseluruhan, spektroskopi Raman in situ Ni 3 Mo selaras dengan daerah potensial dari tahap transformasi fase yang disarankan pada Gambar 3b .
Untuk katalis Ni3Mo @ Cx , potensial yang diperlukan untuk transformasi dari Ni metalik menjadi α-Ni(OH) 2 bergeser ke nilai yang lebih tinggi dengan peningkatan waktu perlakuan CO. (Gambar S11b , Informasi Pendukung) Posisi puncak transformasi fase bergeser dari 0,75 V RHE untuk Ni3Mo @ C10 menjadi 0,92 V RHE untuk Ni3Mo @ C300 , yang menunjukkan bahwa kulit karbon menghambat transformasi oksidatif, yang membutuhkan kelebihan potensial berlebih agar oksidasi dapat terjadi. Pergeseran ini memperluas jendela potensial untuk fase metalik (tahap I), yang memungkinkan katalis Ni3Mo @ Cx mempertahankan sifat metalik dan aktivitas HER bahkan setelah 1 jam penuaan di bawah sirkuit terbuka dalam 1 m KOH (Gambar 2a ).
Kehilangan aktivitas HER setelah transformasi menjadi hidroksida dan peran kulit karbon dalam retensi aktivitas telah dikonfirmasi dengan memaparkan katalis Ni 3 Mo dan Ni 3 Mo@C 60 pada tahap transformasinya masing-masing dengan rentang CV yang bervariasi (Gambar S14 , Informasi Pendukung). Kedua katalis tidak menunjukkan degradasi yang jelas hingga 0,05 V RHE (tahap I), sementara kehilangan aktivitas yang substansial untuk Ni 3 Mo diamati ketika didaur ulang hingga 0,55 V RHE (tahap II, melampaui puncak pembentukan hidroksida) dan kehilangan aktivitas yang lengkap ketika didaur ulang hingga 1,05 V RHE (tahap III) atau 1,55 V RHE (tahap V). Di sisi lain, Ni 3 Mo@C 60 tidak menunjukkan kehilangan aktivitas ketika dinaikkan siklusnya hingga 0,55 V RHE (tahap I), dengan sedikit kehilangan aktivitas ketika dinaikkan siklusnya hingga 1,05 V RHE (tahap III, melampaui puncak pembentukan hidroksida), dan hanya mengalami kehilangan aktivitas sedang bahkan ketika dinaikkan siklusnya hingga 1,55 V RHE (tahap V).
Transformasi struktural antara berbagai fase Ni disertai dengan perubahan volumetrik substansial (Gambar 3c ). Ni metalik memiliki volume spesifik 112,3 cm3 mg − 1 , sedangkan α-Ni(OH) 2 memiliki volume spesifik yang jauh lebih tinggi yaitu 354,6 cm3 mg − 1 . Transformasi Ni metalik3Mo ke fase hidroksidanya memerlukan ekspansi volumetrik yang signifikan. Di sisi lain, kulit karbon katalis Ni3Mo @ Cx secara sterik menekan ekspansi volumetrik ini, mencegah transformasi oksidatif dari logam menjadi hidroksida. Sementara kulit karbon yang rusak memungkinkan difusi molekul air dan anion hidroksida untuk HER, kulit karbon mencegah penggabungan ion hidroksida ke dalam kisi logam untuk transformasi ke fase hidroksida. Klaim ini didukung oleh pola XRD Ni3Mo@C60 yang tidak berubah setelah penuaan dalam 1 M KOH, sedangkan Ni3Mo mengembangkan pola difraksi yang sesuai dengan β-Ni(OH) 2 (Gambar 3d ). Gambar TEM dari Ni3Mo yang menua memperlihatkan pelat besar, tetapi Ni3Mo @C60 yang menua tidak memperlihatkan perubahan morfologi yang signifikan (Gambar S15 , Informasi Pendukung). Sementara pemetaan ICP-MS dan EDS memperlihatkan kehilangan Mo untuk kedua katalis yang diperoleh setelah penyaringan, kehilangan tersebut lebih jelas untuk Ni3Mo ( Tabel S6 , Informasi Pendukung).
Tingkat transformasi fase pada permukaan diselidiki lebih lanjut dengan menganalisis spektrum Ni 2p XPS dari Ni 3 Mo dan Ni 3 Mo@C 60 setelah penuaan dalam 1 M KOH (Gambar S16 , Informasi Pendukung). Oksidasi permukaan yang substansial diamati untuk kedua katalis, dengan hanya 2,3% Ni valensi nol (Ni 0 ) yang tersisa dalam Ni 3 Mo dan 7,2% dalam Ni 3 Mo@C 60 . Untuk menyelidiki perbedaan dalam tingkat oksidasi, Ni 2p XPS diukur ulang setelah sputtering Ar + selama 1 menit. Ni 3 Mo menunjukkan 28,2% Ni 0 sementara Ni 3 Mo@C 60 menyajikan 66,0% Ni 0 . Hasil XPS menunjukkan bahwa oksidasi permukaan ditekan secara signifikan dengan enkapsulasi cangkang karbon dalam Ni 3 Mo@C x , membatasinya ke permukaan terluar.
Agar oksidasi elektrokimia Ni metalik menjadi α-Ni(OH) 2 (transisi tahap I/II) berlangsung, ion OH − harus berdifusi melalui kulit karbon yang rusak dan teradsorpsi pada permukaan logam Ni. Energi adsorpsi OH dihitung dengan teori fungsi kerapatan (DFT) menjadi −4,01 eV pada Ni 3 Mo dan −2,02 eV pada Ni 3 Mo@C x , berturut-turut (Gambar S17 , Informasi Pendukung). Energi ikatan yang lebih negatif berhubungan dengan ikatan yang lebih kuat antara OH dan permukaan katalis. Kulit karbon mengurangi kerentanan permukaan Ni untuk teroksidasi. Pengukuran desorpsi terprogram suhu (TPD) dan spektroskopi inframerah transformasi Fourier (FT-IR) dilakukan untuk menyelidiki pembentukan spesies hidroksida pada permukaan Ni 3 Mo dan Ni 3 Mo@C 60 ketika mereka menua dalam 1 m KOH selama 24 jam (Gambar S18 , Informasi Pendukung). Sementara Ni 3 Mo yang sudah tua menampilkan puncak-puncak tajam yang sesuai dengan spesies hidroksida permukaan, Ni 3 Mo@C 60 yang sudah tua hampir tidak menampilkan puncak semacam itu, yang mengindikasikan bahwa kulit karbon pasti menghambat pembentukan hidroksida.
Untuk memantau proses transformasi, operando Ni K-edge XANES dilakukan untuk Ni 3 Mo dan Ni 3 Mo@C 60 dalam 1 M KOH di bawah OCV menggunakan sel aliran buatan lab (Gambar 3e ; Gambar S19 , Informasi Pendukung). Intensitas garis putih Ni 3 Mo meningkat secara signifikan dengan pemindaian berulang, yang menunjukkan oksidasi Ni. [ 22 ] Perubahan pada fitur pra-tepi K, yang dikaitkan dengan simetri koordinasi lokal pusat Ni, menunjukkan pembentukan ikatan Ni-O untuk mengonfirmasi transformasi oksidatif menjadi α/β-Ni(OH) 2 di bawah sirkuit terbuka. [ 38 ] Selain itu, perubahan osilasi pasca-tepi, yang mencerminkan penataan ulang geometri di sekitar atom Ni, memberikan bukti lebih lanjut tentang transformasi. [ 39 ] Ni 3 Mo@C 60 , bagaimanapun, menunjukkan perubahan minimal pada fitur-fitur ini, yang menunjukkan bahwa cangkang karbon secara efektif menekan transformasi fase dan mempertahankan sifat logam awal di bawah sirkuit terbuka dalam 1 m KOH (Gambar 3e ).
Secara kolektif, analisis elektrokimia, ex-situ, komputasional, dan struktur operando menunjukkan bahwa cangkang karbon katalis Ni3Mo @ Cx mencegah oksidasi inti logam dengan menekan ekspansi kisi logam volumetrik dalam media alkali. Hal ini memungkinkan katalis untuk mempertahankan aktivitas HER dengan menstabilkan fase logam yang aktif terhadap HER sambil menekan pembentukan β-Ni(OH) 2 yang tidak aktif terhadap HER dalam 1 m KOH.
2.3 AEMWE Terintegrasi dengan Elektroda Referensi
Sementara analisis elektrokimia setengah sel memberikan wawasan berharga ke dalam aktivitas katalis dan mekanisme deaktivasi, sering kali gagal dalam memprediksi kinerja mereka dalam elektroliser air dalam kondisi operasional praktis. [ 40 – 42 ] Akibatnya, sangat penting untuk mengevaluasi aktivitas katalis dan daya tahan dalam rakitan elektroda membran (MEA) untuk mencerminkan skenario yang realistis. Namun, MEA konvensional memiliki dua elektroda terpolarisasi yang digabungkan (katoda dan anoda), yang mempersulit evaluasi katalis HER atau OER individual yang andal. Untuk mengatasi tantangan ini, berbagai penelitian telah mengusulkan dengan mengintegrasikan elektroda referensi yang tidak terpolarisasi ke dalam MEA. [ 43 – 52 ] Namun, desain sebelumnya, terutama untuk AEMWE, telah menemui keterbatasan, termasuk pemutusan elektroda penginderaan, penyimpangan potensial, dan nilai potensial referensi yang tidak dapat diandalkan pada kerapatan arus tinggi, yang membatasi penerapannya pada kondisi tertentu. [ 43 , 48 ] Mungkin karena tantangan-tantangan ini, sejauh pengetahuan kami, belum ada penelitian sebelumnya yang menunjukkan pemantauan berkelanjutan terhadap potensi anoda dan katoda individual selama uji ketahanan pada AEMWE menggunakan elektroda referensi terintegrasi.
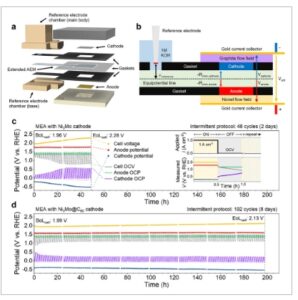
Bahasa Indonesia: Untuk memanfaatkan keuntungan dari titik referensi non-polarisabel yang stabil, AEMWE yang terintegrasi dengan elektroda referensi dikembangkan (Gambar S20 , Informasi Pendukung). Desain ini, terinspirasi oleh Boettcher et al., [ 43 ] menggunakan membran pertukaran anion yang diperluas untuk menghubungkan MEA secara ionik ke ruang elektroda referensi eksternal. Persiapan MEA melibatkan elemen desain yang presisi, termasuk membran berbentuk khusus dan gasket tambahan untuk menghilangkan potensi kebocoran elektrolit, memastikan konektivitas yang stabil selama ratusan jam ( Gambar 4 a ). Ruang eksternal menampung elektroda hidrogen reversibel (Hydroflex, Gaskatel) yang direndam dalam 1 m KOH, terhubung secara ionik ke MEA melalui wilayah membran yang diperluas, yang berfungsi sebagai kapiler Luggin untuk merasakan medan listrik antara elektroda planar (Gambar 4b ).
Gambar 4
Buka di penampil gambar
Kekuatan Gambar
AEMWE terintegrasi dengan elektroda referensi dan kinerja MEA dengan katalis katode Ni 3 Mo dan Ni 3 Mo@C 60 dalam protokol intermiten. a) Tampilan terurai AEMWE terintegrasi dengan elektroda referensi. b) Skema yang menunjukkan prinsip kerja di balik penginderaan medan listrik antara katode dan anoda oleh elektroda referensi. Tegangan sel dan potensial elektroda pada 1 A cm −2 dan dalam rangkaian terbuka selama protokol intermiten menggunakan (c) Ni 3 Mo dan (d) Ni 3 Mo@C 60 . Gambar sisipan dalam (c) menunjukkan protokol intermiten yang digunakan untuk menguji MEA, yang terdiri dari siklus berulang kronopotensiometri selama 30 menit pada 1 A cm −2 dan OCV selama 30 menit.
Selain itu, daripada menggunakan membran tipis (10–20 µm) dan suhu operasi tinggi (≈80 °C) untuk mencapai kerapatan arus awal yang tinggi, dipilih membran yang cukup tebal (60 µm) dan suhu operasi sedang (50 °C). Pendekatan ini memastikan stabilitas membran dan ionomer yang memadai, sehingga memungkinkan evaluasi yang andal dengan fokus pada stabilitas katalis di berbagai protokol operasi. [ 53 ]
Dengan menggunakan pengaturan ini, katalis katode Ni3Mo atau Ni3Mo @ C60 dan katalis anoda NiFe layered double hydroxides (LDH) dievaluasi secara individual dengan memisahkan sinyal elektrokimia dalam MEA di bawah protokol ketahanan kontinu dan intermiten. Protokol kontinu terdiri dari kronopotensiometri pada 1 A cm −2 selama 24 jam. Di bawah protokol ini, degradasi minimal diamati untuk MEA dengan Ni3Mo , dengan tegangan sel hanya meningkat sedikit dari 1,98 V pada awal masa pakai (BoL) menjadi 2,01 V pada akhir masa pakai (EoL) (Gambar S21 , Informasi Pendukung). Potensial elektroda yang dipisahkan mengonfirmasi kinerja anoda yang stabil dan hanya degradasi katode yang minor, yang menunjukkan bahwa katalis tersebut kuat dalam operasi yang stabil.
Protokol intermiten melibatkan operasi 30 menit secara bergantian pada 1 A cm −2 dengan 30 menit istirahat pada OCV, diulang hingga 192 siklus (8 hari). Di bawah protokol ini, MEA dengan katode Ni 3 Mo menunjukkan degradasi yang signifikan, karena tegangan sel meningkat dari 1,96 V pada BoL menjadi 2,28 V pada EoL pada 1 A cm −2 setelah 48 siklus (2 hari) (Gambar 4c ; Gambar S22a , Informasi Pendukung). Menariknya, potensial anoda tetap stabil selama kondisi kronoamperometri dan sirkuit terbuka, sedangkan potensial katode menunjukkan peningkatan yang nyata. Stabilitas NiFe LDH yang luar biasa sebagai katalis anoda dalam kondisi intermiten dikaitkan dengan transformasi yang sangat reversibel antara fase α-hidroksida inert OER dan fase γ-oksihidroksida aktif OER. [ 35 ] Sebaliknya, transformasi ireversibel Ni3Mo metalik yang aktif HER menjadi hidroksida yang tidak aktif HER selama periode OCV, sebagaimana dibuktikan oleh peningkatan terus-menerus dalam potensial katode, merupakan sumber utama degradasi. MEA dengan katode Ni3Mo @ C60 menunjukkan daya tahan yang luar biasa dalam kondisi yang sama (Gambar 4d ; Gambar S22b , Informasi Pendukung). Tegangan sel hanya meningkat sedikit, dari 1,99 V (BoL) menjadi 2,13 V (EoL), meskipun pengujian daya tahan diperpanjang sebanyak 192 siklus (8 hari). Khususnya, potensial katode Ni3Mo @ C60 pada keadaan diam (sirkuit terbuka) dengan cepat menjadi stabil dan tetap di bawah ≈0,3 V RHE , jauh di bawah wilayah potensial yang terkait dengan pembentukan hidroksida.
Lapisan katode diamati dengan SEM setelah uji ketahanan dalam kondisi intermiten (Gambar S23 , Informasi Pendukung). Sementara katode Ni3Mo EoL menunjukkan pembentukan β-Ni(OH) 2 yang ekstensif , transformasi tersebut tidak ada untuk Ni3Mo @ C60 , yang mengonfirmasi bahwa lapisan karbon secara efektif menekan pembentukan hidroksida. Struktur skala nano mereka selanjutnya diamati menggunakan HR-TEM dan STEM. Sementara sebagian besar Ni3Mo menunjukkan transformasi menjadi struktur seperti platelet setelah 48 siklus (Gambar S24 , Informasi Pendukung), Ni3Mo @ C60 mempertahankan morfologi partikel aslinya yang menunjukkan keberadaan cangkang karbon utuh yang membungkus inti logam bahkan setelah 192 siklus (Gambar S25 , Informasi Pendukung). Pengoperasian sel juga dipantau oleh spektroskopi impedansi elektrokimia (EIS), dan hal ini memperjelas bahwa peningkatan resistansi pemindahan muatan katode merupakan pendorong degradasi utama untuk MEA dengan Ni 3 Mo (Gambar S26a , Informasi Pendukung). Sebagai perbandingan, Ni 3 Mo@C 60 menunjukkan peningkatan resistansi pemindahan muatan yang jauh lebih rendah, yang menguatkan peningkatan stabilitasnya (Gambar S26b , Informasi Pendukung).
Elektroda referensi terintegrasi memungkinkan evaluasi ketat kinerja MEA dengan memisahkan asal-usul overpotensial ( Gambar 5 ). Kurva IV yang diperoleh selama protokol intermiten dianalisis menggunakan koreksi resistansi frekuensi tinggi (HFR) untuk menghilangkan penurunan tegangan ohmik (Gambar 5a,b ). Analisis Tafel dari kurva iV yang dikoreksi HFR di wilayah kinetik dilakukan untuk menentukan kemiringan Tafel untuk setiap kurva, yang memungkinkan perhitungan overpotensial kinetik pada masing-masing elektroda (Gambar S27 dan Tabel S7 , Informasi Pendukung). Pendekatan komprehensif ini memungkinkan decoupling menjadi beberapa komponen overpotensial, termasuk potensial termodinamika untuk elektrolisis air, overpotensial ohmik dari resistansi membran, dan overpotensial kinetik dan transpor massa individual untuk katode dan anoda.

Gambar 5
Buka di penampil gambar
Kekuatan Gambar
Kurva iV awal masa pakai (BoL) dan akhir masa pakai (EoL) setelah koreksi menggunakan resistansi frekuensi tinggi (HFR) untuk MEA dengan (a) Ni 3 Mo dan (b) Ni 3 Mo@C 60 katalis katode. Protokol intermiten sama seperti pada Gambar 4. Dekopling overpotensial untuk MEA dengan Ni 3 Mo pada (c) BoL dan (d) EoL, dan dengan Ni 3 Mo@C 60 pada (e) BoL dan (f) EoL. Kurva iV EoL diukur setelah 48 siklus protokol intermiten untuk Ni 3 Mo dan setelah 192 siklus untuk Ni 3 Mo@C 60 .
Analisis overpotensial terperinci mengungkapkan bahwa overpotensial kinetik pada katode Ni 3 Mo meningkat tajam selama protokol intermiten 2 hari, yang akhirnya menjadi kontributor dominan terhadap tegangan sel berlebih (Gambar 5c,d ). Sebaliknya, untuk Ni 3 Mo@C 60 , overpotensial kinetik pada katode awalnya lebih besar daripada Ni 3 Mo, tetapi overpotensial hanya sedikit meningkat setelah protokol intermiten 8 hari (Gambar 5e,f ). Perbandingan kontribusi overpotensial pada 1 A cm −2 untuk MEA dengan Ni 3 Mo dan Ni 3 Mo@C 60 sebelum dan sesudah protokol intermiten dengan jelas menggambarkan perbedaan dalam profil degradasi (Gambar S28 , Informasi Pendukung).
Temuan ini menyoroti peran penting enkapsulasi karbon dalam mencegah penonaktifan katalis yang ireversibel dari paduan NiMo dalam kondisi AEMWE yang terputus-putus. Penggabungan elektroda referensi ke dalam AEMWE memungkinkan pemisahan yang tepat dari kontribusi tegangan berlebih, yang menawarkan wawasan berharga tentang mekanisme degradasi dan memungkinkan penilaian yang ketat terhadap ketahanan katalis dalam kondisi operasi yang realistis.
3 Kesimpulan
Pekerjaan ini menyelidiki mekanisme degradasi dan strategi mitigasi untuk katalis HER berbasis NiMo dalam AEMWE dalam kondisi operasi intermiten. Dengan mensintesis dan mengkarakterisasi paduan NiMo berkapsul karbon (Ni3Mo @ Cx ) , kami menunjukkan bahwa cangkang karbon yang rusak mempertahankan integritas logam inti Ni3Mo . Cangkang karbon ini secara efektif menekan transformasi oksidatif ireversibel dari Ni logam menjadi fase hidroksida HER-inaktif, didorong oleh ekspansi kisi volumetrik dalam kondisi OCV dalam elektrolit KOH 1 m . Evaluasi elektrokimia dalam operasi intermiten mengonfirmasi stabilitas katalis berkapsul karbon, dengan degradasi minimal yang diamati bahkan setelah siklus intermiten yang diperpanjang selama 8 hari. Khususnya, integrasi elektroda referensi ke dalam AEMWE memungkinkan pemisahan kontribusi tegangan lebih, mengungkapkan bahwa degradasi katoda NiMo adalah penyebab utama penurunan kinerja sel secara keseluruhan dalam kondisi intermiten, bukan degradasi anoda. Temuan ini menyoroti pentingnya memastikan stabilitas katalis HER di katode untuk mencapai operasi AEMWE yang stabil dan terputus-putus. Secara keseluruhan, studi ini menawarkan jalur yang menjanjikan untuk mencapai produksi hidrogen yang hemat biaya dan tahan lama menggunakan sistem AEMWE bebas PGM, terutama dalam skenario energi terbarukan yang terputus-putus.
4 Bagian Eksperimen
Bahan kimia
Nikel (II) klorida heksahidrat (NiCl2 · 6H2O , 99,999% basis logam), molibdenum klorida (MoCl5 , 95%), natrium hidroksida (NaOH, ≥ 97%), natrium karbonat (Na2CO3 , ≥ 99,5%), besi klorida (FeCl3 , 97%), dan larutan resin perfluorinasi Nafion (5 wt.% dalam alkohol alifatik rendah/air ) diperoleh dari Sigma-Aldrich. 2-propanol ((CH3 ) 2CHOH , 99,7%) dibeli dari Junsei. Membran pertukaran anion PiperION (PiperION-A60-HCO3, Versogen), kertas karbon Toray Paper 090 (TGP-H-090), dan busa Nikel (80-120 PPI – 1 mm) dibeli dari Fuel Cell Store. Semua bahan kimia digunakan sebagaimana mestinya tanpa pemurnian lebih lanjut. Air deionisasi (18,2 MΩ·cm) digunakan untuk semua percobaan.
Sintesis Katalis
Larutan prekursor logam homogen dibuat dengan melarutkan 6,417 g NiCl2 · 6H2O dan 2,459 g MoCl5 dalam 45 mL air deionisasi (rasio molar 3:1). Secara terpisah, larutan alkali dibuat dengan melarutkan 3,060 g NaOH dan 2,623 g Na2CO3 dalam 45 mL air deionisasi. Kedua larutan ditambahkan tetes demi tetes ke dalam 90 mL air deionisasi sambil diaduk, pertahankan pH sekitar 8,5. Campuran yang dihasilkan didiamkan semalaman, dicuci bersih dengan air deionisasi dan etanol, dan dikeringkan pada suhu 60 °C. Bubuk prekursor Ni3Mo-hidroksida yang diperoleh digiling dan disimpan dalam desikator vakum. Sekitar 330 mg prekursor ditempatkan dalam wadah alumina di dalam tungku tabung. Suhu dinaikkan ke 330 °C pada 10 °C min -1 dan ditahan selama 40 menit dalam atmosfer H 2 /N 2 (6,5/156 sccm). Produk kemudian didinginkan ke suhu kamar di bawah aliran N 2 , maka katalis Ni 3 Mo diperoleh. Katalis Ni 3 Mo yang dienkapsulasi karbon (Ni 3 Mo@C x ) disintesis dengan memasukkan gas CO ke katalis Ni 3 Mo. Setelah reduksi, katalis diekspos ke CO (156 sccm) pada 330 °C dengan durasi yang bervariasi (10 – 300 menit). Katalis kemudian didinginkan ke suhu kamar di bawah aliran N 2 . Durasi perlakuan CO ditunjukkan dalam nama katalis (misalnya, Ni 3 Mo@C 60 selama 60 menit).
Katalis NiFe LDH disintesis sebagai katalis OER, mengikuti pekerjaan kami sebelumnya. [ 54 ] Larutan prekursor logam disiapkan dengan melarutkan 6,417 g NiCl2 · 6H₂O dan 1,459 g FeCl3 dalam 45 mL air deionisasi. Larutan alkali disiapkan seperti yang dijelaskan untuk sintesis Ni3Mo hidroksida . Kedua larutan ditambahkan tetes demi tetes ke dalam 90 mL air deionisasi sambil diaduk, pertahankan pH ≈8,5. Campuran yang dihasilkan disimpan semalaman, dicuci dengan air deionisasi dan etanol, dan dikeringkan pada suhu 60 °C. Bubuk kering digiling dan digunakan secara langsung.
Karakterisasi
Mikroskopi elektron transmisi (TEM; FEI Tecnai G2 F30 S-Twin) dilakukan menggunakan berkas elektron 300 kV. Difraktometer sinar-X (XRD; SmartLab, Rigaku) digunakan untuk memperoleh pola difraksi sinar-X serbuk beresolusi tinggi. Kandungan unsur Ni dan Mo dalam katalis diukur menggunakan spektrometri massa plasma yang diinduksi (ICP-MS; Perkin Elmer NexION 1000). TPO dan TPD dilakukan menggunakan BELCAT-B (MicrotracBEL) yang dilengkapi dengan spektrometer massa (BELMASS). 50 mg serbuk katalis diolah terlebih dahulu dengan 50 sccm He pada suhu 45 °C selama 1 jam. Untuk TPO, suhu dinaikkan hingga 900 °C di bawah gas O 2 /He 5% pada suhu 10 °C min −1 . Untuk TPD, suhu dinaikkan ke 900 °C di bawah aliran He kontinu pada 10 °C min −1 . Spektrum Raman ex-situ dari bubuk katalis Ni 3 Mo@C x diperoleh menggunakan spektroskop Raman confocal (Nanobase XperRam S) dengan panjang gelombang laser 523 nm dan daya laser 9,2 mW. Mikroskop dengan lensa perbesaran 50 dan kisi 1800 alur per 1 mm digunakan. Spektroskopi fotoelektron sinar-X (XPS; Thermo VG Scientific, K-alpha) digunakan untuk mengukur komposisi permukaan katalis. Sputtering Ar + dilakukan selama 1 menit dengan energi ion 2 kV, dengan ukuran raster sputter 2 mm. Ion klaster (Ar + n ) digunakan untuk meminimalkan kerusakan permukaan. Energi pengikatan dikoreksi menggunakan intensitas maksimum sinyal referensi C 1 s pada 284,8 eV. Mikroskopi elektron pemindaian (SEM; Hitachi SU5000) dan spektroskopi sinar-X dispersif energi (EDS) dilakukan untuk mengamati morfologi dan permukaan elektroda. FT-IR dilakukan menggunakan instrumen Nicolet iS-50 (Thermo Scientific) dengan jendela KBr. Katalis dicampur dengan bubuk KBr, digiling secara menyeluruh, dimasukkan ke dalam cawan sampel, dan ditempatkan di sel sampel. Sebelum pengukuran, sampel diolah terlebih dahulu pada suhu 100 °C selama 1 jam di bawah atmosfer Ar. Spektrum direkam di bawah Ar untuk menghindari gangguan sekitar.
Pengukuran spektroskopi Raman in situ dilakukan menggunakan mikroskop Raman confocal InVia Qontor (RENISHAW) dengan laser 532 nm dan sel elektrokimia yang dibuat khusus melalui lensa objektif perendaman air 63x. Waktu paparan adalah 20 detik dengan 3 kondisi akumulasi. Di bawah sistem tiga elektroda, katalis Ni 3 Mo dilapisi semprot pada kertas karbon dan digunakan sebagai elektroda kerja. Kawat Pt dan Hg/HgO (1 M KOH) digunakan sebagai elektroda lawan dan referensi, masing-masing, dalam 1 M KOH. Untuk memperoleh spektrum Raman dalam kondisi kondisi tunak pada berbagai potensial yang diterapkan, kronoamperometri multi-langkah dilakukan pada setiap potensial selama sapuan anodik (0 V RHE hingga 1,45 V RHE ) dan sapuan katoda (1,45 V RHE hingga 0 V RHE ).
Spektroskopi serapan sinar-X (XAS) dilakukan pada garis sinar XAFS selebar 10 C dari Sumber Cahaya Pohang. Spektrum tepi Ni dan Mo K dari katalis bubuk diperoleh dalam mode transmisi. Spektrum tepi operando Ni K dari lapisan katalis diperoleh dalam mode fluoresensi. Sel aliran buatan laboratorium yang dipasang pada pompa diafragma (SIMDOS 02, KNF) digunakan untuk mengalirkan 1 M KOH ke lapisan katalis. Lembaran grafena (Graphene Supermarket), kawat Pt, dan elektroda Hg/HgO masing-masing digunakan sebagai elektroda kerja, elektroda lawan, dan elektroda referensi. Beban katalis adalah 0,25 mg logam cm −2 . Semua pengukuran dikalibrasi menggunakan foil logam referensi. Data XAS diproses dengan program perangkat lunak ATHENA untuk memperoleh spektrum EXAFS berbobot XANES dan k3 . Semua pengukuran elektrokimia dilakukan menggunakan VSP-300 (Biologic) dengan penguat arus tambahan 10 A / 5 V.
Pengukuran Setengah Sel
Pengukuran elektrokimia setengah sel dilakukan dalam pengaturan tiga elektroda dengan elektroda cakram berputar karbon kaca (RDE, PINE) sebagai elektroda kerja, batang karbon sebagai elektroda lawan, dan elektroda hidrogen reversibel (RHE, Hydroflex, Gaskatel) sebagai elektroda referensi pada 1600 rpm dan suhu ruangan. 1 M KOH digunakan sebagai elektrolit setelah dibersihkan dengan gas Ar untuk memastikan atmosfer inert. Khususnya, 1 M KOH bebas Fe disiapkan mengikuti prosedur yang dilaporkan sebelumnya, [ 28 ] dan larutan elektrolit bebas Fe ini digunakan untuk semua pengukuran dalam pekerjaan ini. Tinta katalis disiapkan dengan mendispersikan 5 mg katalis dan 1,25 mg karbon Vulkan dalam 2 mL isopropanol, 0,5 mL air deionisasi, dan 20 µL dispersi ionomer Nafion. Setelah disonikasi selama 30 menit, 9,90 µL tinta diteteskan ke RDE, sehingga menghasilkan muatan katalis sebesar 0,10 mg cm −2 . Untuk mencegah penonaktifan katalis berbasis Ni, potensial 0 V RHE segera diterapkan saat elektroda kerja direndam dalam elektrolit. Aktivitas awal katalis diperoleh dengan LSV dari 0 V RHE hingga −0,45 V RHE pada laju pindai 10 mV s −1 . Potensial pada rangkaian terbuka diukur selama 60 menit, kemudian LSV lain dilakukan. CV dilakukan dari 0 V RHE hingga 1,55 V RHE selama 2 siklus pada laju pindai 10 mV s −1 untuk mengamati transformasi fase Ni. EIS pada 0 V RHE dilakukan setelah setiap LSV untuk koreksi iR manual .
AEMWE Terintegrasi dengan Elektroda Referensi
Pengukuran AEMWE dilakukan menggunakan pengaturan sel tunggal komersial (Fuel Cell Technologies) yang terintegrasi dengan ruang elektroda referensi yang dirancang khusus. Tinta katalis katode disiapkan dengan mendispersikan 156,25 mg Ni3Mo atau Ni3Mo @ C60 dan 39,06 mg karbon Vulcan ke dalam larutan 12,5 mL isopropil alkohol, 3,125 mL air deionisasi, dan 0,913 mL ionomer PiperION 5 wt%. Campuran tersebut diultrasonikasi selama 1 jam, kemudian disemprotkan ke kertas karbon yang diletakkan di atas pelat panas yang dipanaskan hingga 80 °C. Kertas karbon berlapis katalis dipotong untuk berfungsi sebagai katode, dengan target pemuatan katalis sebesar 2,0 mg cm −2 . Tinta katalis anoda disiapkan dengan mendispersikan 156,25 mg NiFe LDH ke dalam larutan 12,5 mL isopropil alkohol, 3,125 mL air deionisasi, dan 0,913 mL ionomer PiperION 5 wt%. Tinta ini juga diultrasonikasi selama 1 jam dan disemprotkan ke busa Ni pada pelat panas yang dipanaskan hingga 80 °C. Busa Ni yang dilapisi katalis dipotong untuk berfungsi sebagai anoda, dengan target pemuatan katalis sebesar 2,5 mg cm −2 . Rakitan elektroda membran (MEA) dibuat pada perangkat keras sel tanpa pengepresan panas. Tiga gasket, berbentuk seperti yang diilustrasikan pada Gambar 4a , digunakan untuk mencegah kebocoran elektrolit. Membran pertukaran anion PiperION dipotong agar sesuai dengan paking tengah, diaktifkan dalam 1 M KOH selama 1 jam, dibilas dengan air deionisasi, dan ditempatkan di antara katode dan anoda pada blok grafit dan Ni, masing-masing memiliki pola aliran berkelok-kelok tunggal. Sel dirakit dengan torsi 50 kgf·cm dan dipanaskan hingga 50 °C menggunakan batang pemanas terintegrasi. Area aktif MEA adalah 5 cm2 . Ruang elektroda referensi dibuat menggunakan PEEK untuk menahan elektroda hidrogen reversibel (Hydroflex, Gaskatel) yang direndam dalam 1 M KOH. Konektivitas ionik antara elektroda referensi dan MEA dipertahankan menggunakan bagian yang diperpanjang dari membran pertukaran anion, seperti yang digambarkan pada Gambar 4b . Reservoir terpisah yang berisi 0,5 L KOH 1 M digunakan sebagai katolit dan anolit. Kedua elektrolit dipanaskan hingga 50 °C dan dialirkan pada laju aliran 25 mL menit −1 menggunakan pompa peristaltik.
Protokol Pengujian Aktivitas dan Daya Tahan di AEMWE
MEA diaktifkan menggunakan kronopotensiometri pada 0,05 A cm −2 hingga kinerjanya stabil. Selanjutnya, kurva iV direkam dengan menahan setiap kerapatan arus selama 1 menit, berkisar dari 0,02 hingga 1,5 A cm −2 pada interval tertentu. Spektroskopi impedansi elektrokimia galvanostatik (GEIS) dilakukan pada 50 mA cm −2 dari 100 kHz hingga 0,1 Hz dengan amplitudo 10 mV setelah setiap pengukuran iV untuk mengukur resistansi frekuensi tinggi (HFR). Daya tahan diuji di bawah dua protokol. Protokol berkelanjutan melibatkan kronopotensiometri pada 1 A cm −2 selama 24 jam, sedangkan protokol terputus-putus terdiri dari siklus berulang selama 30 menit pada 1 A cm −2 diikuti oleh 30 menit pada OCV. Siklus ini diulang hingga 192 kali (8 hari, 192 jam). Degradasi dinilai dengan memperoleh kurva iV setiap 24 siklus.
Perhitungan Teori Fungsi Kepadatan (DFT)
Semua perhitungan DFT yang digunakan dalam studi ini dilakukan oleh paket simulasi Vienna ab initio (VASP). [ 55 ] Metode gelombang tertambah proyektor (PAW) digunakan untuk merepresentasikan interaksi inti-elektron valensi. [ 56 ] Energi pertukaran dan korelasi dihitung dengan revisi fungsional Perdew-Burke-Ernzehof (rPBE) dalam aproksimasi gradien umum (GGA). [ 57 ] Semua perhitungan dilakukan dengan energi batas gelombang bidang 400 eV dan pengambilan sampel k -titik 3 × 3 × 1 dengan skema Monkhorst-Pack. Konvergensi komputasional berada dalam 10 −5 eV dan 0,05 eV A −1 untuk energi dan gaya, masing-masing. Untuk semua perhitungan, efek polarisasi spin dipertimbangkan. Untuk interaksi antara lapisan graphene, metode DFT-D3 digunakan untuk koreksi gaya van der Waals. Ruang vakum tegak lurus 15 Å digunakan untuk memastikan bahwa sistem memiliki sedikit interaksi dengan gambarnya. Permukaan Ni 3 Mo(101) dimodelkan menggunakan lempengan sel satuan 2 × 2 dengan enam lapisan atom. [ 20 ] Untuk memperhitungkan cangkang karbon, dua lapisan grafena ditempatkan di atas permukaan Ni 3 Mo(101). 40 atom karbon per lapisan digunakan dalam supersel untuk memastikan simetri dalam batas periodik. Energi pengikatan ( E b ) dari ion hidroksil dan permukaan katalis dihitung dengan persamaan berikut: E b = E adsorbat/katalis – E adsorbat – E katalis , di mana E adsorbat/katalis , E adsorbat , dan E katalis masing-masing berkorespondensi dengan energi total katalis yang diadsorpsi oleh spesies kimia di permukaan, energi total adsorbat yang terisolasi, dan katalis yang bersih. E b yang lebih negatif berkorespondensi dengan ikatan yang lebih kuat antara ion hidroksil dan permukaan katalis.

